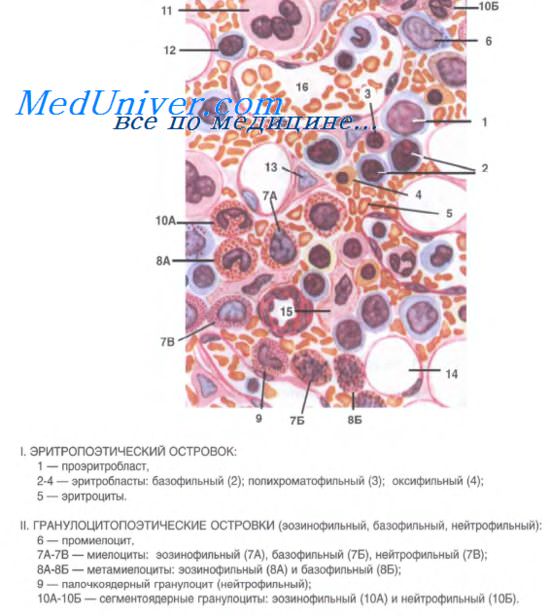
Паренхима красного костного мозга образована
К системе реактивности организма человека принадлежат органы, осуществляющие восприятие всех внешних и внутренних сигналов, их анализ и адекватную конкретной обстановке регуляцию жизнедеятельности, а также интеграцию функций органов и систем организма. Систему реактивности представляют органы иммунной защиты, эндокринные железы, нервная система с ее периферическим сенсорным аппаратом. Эти три части организма объединяются в единую нейро-эндокринно-иммунную систему, поскольку их деятельность взаимно согласована и зависима. Так, нейропептиды, синтезируемые эндокринными нейронами, влияют на активность иммунокомпетентных клеток, а биологические активные вещества иммунокомпетентных клеток оказывают влияние на клетки и ткани, сходные с таковыми для гормонов эндокриноцитов и пептидов нейронов.
Иммунный комплекс органов
Иммунный комплекс органов включает вилочковую железу (тимус), лимфатические узлы, селезенку, лимфоидные образования в стенке пищеварительного тракта и в других органах и красный костный мозг, где развиваются все клетки крови, в том числе осуществляющие иммунный надзор.
Несмотря на топографическую разобщенность, эти органы вместе с кровью и лимфой образуют единую в функциональном отношении систему, обеспечивающую поддержание процессов кроветворения и иммунной защиты. Органы кроветворения представляют собой открытую систему с постоянным перемещением клеток крови.
Различают центральные и периферические органы кроветворения и иммуногенеза. К центральным органам относят красный костный мозг и вилочковую железу. К периферическим кроветворным и иммунным органам принадлежат лимфатические узлы, селезенка, миндалины и другие лимфоидные образования в составе слизистных оболочек органов.
Красный костный мозг
Красный костный мозг — центральный гемопоэтический орган. В нем находится основная часть стволовых кроветворных клеток и происходит развитие клеток миелоидного и лимфоидного рядов, осуществляется антигеннезависимая дифференцировка В-лимфоцитов (рис. 108).
В эмбриогенезе человека костный мозг появляется впервые на 2-3-м месяцах в плоских костях и позвонках, на 4-м месяце — в трубчатых костях конечностей. Различают красный костный мозг и желтый костный мозг. Красный костный мозг находится в эпифизах трубчатых костей, в губчатом веществе плоских костей, в лопатках, грудине, позвонках, костях черепа. Несмотря на такое рассредоточение, функционально он тесно взаимосвязан благодаря постоянной миграции клеток и наличию общих механизмов регуляции процессов кроветворения.
Масса костного мозга 1,6-3,7 кг, что составляет 3-6% от массы тела. Красный костный мозг имеет темно-красный цвет. Консистенция его полужидкая. Это позволяет делать из него тонкие мазки, изучение которых имеет большое диагностическое значение в клинике.
Строма красного костного мозга образована костными перекладинами, идущими от эндоста. Между ними располагается ретикулярная ткань. Последняя состоит из трехмерной сети гетероморфных ретикулярных клеток фибробластического вида (фибробласты костного мозга). Они вырабатывают межклеточное вещество, включающее ретикулярные волокна и амфорный компонент с большим содержанием гликозаминогликанов, ростовые факторы (интерлейкины). Кроме ретикулярных клеток к стромальным клеточным элементам относятся остеобласты, входящие в состав эндоста и способные влиять на пролиферацию гемопоэтических клеток, адвентициальные — малодифференцированные клетки, сопровождающие кровеносные сосуды, жировые клетки. Все эти клетки развиваются в результате дивергентной дифференцировки стромальной стволовой клетки и играют роль микроокружения для развивающихся клеток крови.
Строма красного костного мозга пронизана кровеносными сосудами микроциркуляторного русла. В основном это капилляры синусоидного типа с диаметром около 30 мкм.
В петлях ретикулярной ткани красного костного мозга расположено множество кроветворных клеток (в том числе стволовых кроветворных, клеток-предшественников миело- и лимфопоэза, клеток гранулоцитарного, эритроцитарного, лимфоцитарного, моноцитарного и тромбоцитарного рядов на различных стадиях дифференцировки).
Количество стволовых кроветворных клеток в красном костном мозге наибольшее по сравнению с другими кроветворными органами (50 на 105 клеток). Концентрация стволовых кроветворных клеток вблизи эндоста в 3 раза больше, чем в других участках костного мозга. Именно здесь наиболее интенсивно идет кроветворение, что связывается с выработкой остеобластами интерлейкинов и повышенным содержанием кальция.
Развивающиеся клетки крови располагаются в красном костном мозге группами (островками, «гнездами»), представляющими собой диффероны, или гистогенетические ряды клеточной дифференцировки. Эритробласты находятся вблизи макрофагов, содержащих железо фагоцитированных эритроцитов, и получают от них железо, необходимое для построения гемоглобина. Созревающие гранулоциты образуют островки, подобно эритроидным клеткам, с тем, однако, отличием, что они не имеют связи с макрофагами.
Клетки тромбоцитарного ряда (мегакариобласты и мегакариоциты) локализуются преимущественно вблизи кровеносных синусоидов. Отростки цитоплазмы мегакариоцитов при этом проникают через поры в стенке синусоидов внутрь сосудов, и от них отделяются фрагменты цитоплазмы в виде кровяных пластинок (тромбоцитов). Последние тут же поступают в кровоток.
В красном костном мозге обычно вокруг кровеносных сосудов встречаются небольшие группы лимфоцитов и моноцитов. Среди множества кровяных клеток в красном костном мозге больше всего зрелых клеточных форм или близких к состоянию зрелости (эритробластов, метамиелоцитов и др.). В случае необходимости, например, при кровопотере, они могут быстро завершить дифференцировку и перейти в кровоток. В нормальных условиях через стенку синусоидных капилляров могут проникать лишь зрелые формы клеточных дифферонов.
Желтый костный мозг расположен в диафизах трубчатых костей. Он представлен преимущественно жировой тканью. В жировых клетках содержится пигмент липохром, имеющий желтый цвет. Желтый костный мозг рассматривается как кроветворный резерв, и в случае больших кровопотерь он начинает функционировать как кроветворный орган. Желтый и красный костный мозг — это два функциональных состояния одного кроветворного органа.
Красный костный мозг очень чувствителен к действию радиации, интоксикаций бензолом, толуолом и другими ядами. Особенно уязвимы при этом «бластные» клеточные формы. Происходит опустошение костного мозга и в результате остается лишь ретикулярная строма. Отмечаются выраженные изменения костного мозга, связанные с превращением миелоидной ткани в жировую, а в старческом возрасте — в слизистую, желатинозную ткани.
Регенерация. Костный мозг обладает высокой регенерационной способностью. После удаления части костного мозга или после облучения ионизирующей радиацией происходит его восстановление за счет заселения костного мозга циркулирующими в крови стволовыми клетками. Необходимым условием при этом является сохранение жизнеспособности стро-мальных клеток. В клинике широко применяют различные методы трансплантации костного мозга.
Анатомия Красного костного мозга человека – информация:
Различают красный костный мозг (medulla ossium rubra) с преобладанием кроветворной миелоидной ткани и жёлтый с преобладанием жировой ткани. Красный костный мозг сохраняется в течение всей жизни в плоских костях (ребрах, грудине, костях черепа, таза), а также в позвонках и эпифазах трубчатых костей. У человека он составляет около 1,5% массы тела. С возрастом кроветворная ткань в полостях трубчатых костей замещается жировой и костный мозг в них становится жёлтым.
Строение красного костного мозга
Масса костного мозга 1,6-3,7 кг, что составляет 3-6% от массы тела. Красный костный мозг имеет темно-красный цвет. Консистенция его полужидкая. Это позволяет делать из него тонкие мазки, изучение которых имеет большое диагностическое значение в клинике. Он содержит стволовые кроветворные клетки (СКК) и диффероны гемопоэтических клеток эритроидного, гранулоцитарного и мегакариоцитарного ряда, а также предшественники В- и Т-лимфоцитов. Стромой костного мозга является ретикулярная соединительная ткань, образующая микроокружение для кроветворных клеток. В настоящее время к элементам микроокружения относят также остеогенные, жировые, адвентициальные, эндотелиальные клетки и макрофаги.
Остеогенными клетками называют стволовые клетки опорных тканей, остеобласты и их предшественники. Остеогенные клетки входят в состав эндоста и могут быть в костномозговых полостях. Остеогенные клетки также способны вырабатывать ростовые факторы, индуцировать родоначальные гемопоэтические клетки в местах своего расположения к пролиферации и дифференцировке. Наиболее интенсивно кроветворение происходит вблизи эндоста, где концентрация стволовых клеток примерно в 3 раза больше, чем в центре костномозговой полости.
Адипоциты (жировые клетки) являются постоянными элементами костного мозга.
Адвентициальные клетки сопровождают кровеносные сосуды и покрывают более 50% наружной поверхности синусоидных капилляров. Под влиянием гемопоэтинов (эритропоэтин) и других факторов они способны сокращаться, что способствует миграции клеток в кровоток.
Эндотелиальные клетки сосудов костного мозга принимают участие в организации стромы и процессов кроветворения, синтезируют коллаген IV типа, гемопоэтины. Эндотелиоциты, образующие стенки синусоидных капилляров, непосредственно контактируют с гемопоэтическими и стромальными клетками благодаря прерывистой базальной мембране. Эндотелиоциты способны к сократительным движениям, которые способствуют выталкиванию клеток крови в синусоидные капилляры. После прохождения клеток в кровоток поры в эндотелии закрываются. Эндотелиоциты выделяют колониестимулирующие факторы (КСФ) и белок фибронектин, обеспечивающий прилипание клеток друг к другу и субстрату.
Макрофаги в костном мозге представлены неоднородными по структуре и функциональным свойствам клетками, но всегда богатыми лизосомами и фагосомами. Некоторые из популяций макрофагов секретируют ряд биологически активных веществ (эритропоэтин, колониестимулирующие факторы, интерлейкины, простагландины, интерферон и др.). Макрофаги при помощи своих отростков, проникающих через стенки синусов, улавливают из кровотока железосодержащее соединение (трансферрин) и далее передают его развивающимся эритроидным клеткам для построения геминовой части гемоглобина.
Гемопоэтические клетки или кроветворные диффероны составляют паренхиму красного костного мозга.
Рассмотрим подробнее образование эритроцитов, гранулоцитов и тромбоцитов в красном костном мозге.
Эритроцитопоэз Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков.
Гранулоцитопоэз Гранулоцитопоэтические клетки также образуют островки, главным образом по периферии костномозговой полости. Незрелые клетки гранулоцитарных рядов окружены протеогликанами. В процессе созревания гранулоциты депонируются в красном костном мозге, где их насчитывается примерно в 3 раза больше, чем эритроцитов, и в 20 раз больше, чем гранулоцитов в периферической крови.
Лимфоцитопоэз и моноцитопоэз Среди островков клеток миелоидного ряда встречаются небольшие скопления костномозговых лимфоцитов и моноцитов, которые окружают кровеносный сосуд. В обычных физиологических условиях через стенку синусов костного мозга проникают лишь созревшие форменные элементы крови. Миелоциты и эритробласты попадают в кровь только при патологических состояниях организма. Причины такой избирательной проницаемости стенки сосудов остаются недостаточно ясными, но факт проникновения незрелых клеток в кровяное русло всегда служит верным признаком расстройства костномозгового кроветворения.
Васкуляризация. Иннервация. Возрастные изменения. Регенерация. Васкуляризация. Костный мозг снабжается кровью посредством сосудов, проникающих через надкостницу в специальные отверстия в компактном веществе кости. Войдя в костный мозг, артерии разветвляются на восходящую и нисходящую ветви, от которых радиально отходят артериолы. Сначала они переходят в узкие капилляры (2-4 мкм), а затем в области эндоста продолжаются в широкие тонкостенные с щелевидными порами синусы (диаметром 10-14 мкм). Из синусов кровь собирается в центральную венулу. Постоянное зияние синусов и наличие щелей в эндотелиальном пласте обусловливаются тем, что в синусах гидростатическое давление несколько повышено, так как диаметр выносящей вены меньше по сравнению с диаметром артерии. К базальной мембране с наружной стороны прилежат адвентициальные клетки, которые, однако, не образуют сплошного слоя, что создает благоприятные условия для миграции клеток костного мозга в кровь. Меньшая часть крови проходит со стороны периоста в каналы остеонов, а затем в эндост и синус.
По мере контакта с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения. Кровеносные сосуды составляют половину (50%) массы костного мозга, из них 30% приходится на синусы. В костном мозге разных костей человека артерии имеют толстую среднюю и адвентициальную оболочки, многочисленные тонкостенные вены, причем артерии и вены редко идут вместе, чаще врозь. Капилляры бывают двух типов: узкие 6-20 мкм и широкие синусоидные (или синусы) диаметром 200-500 мкм. Узкие капилляры выполняют трофическую функцию, широкие являются местом дозревания эритроцитов и выхода в кровоток разных клеток крови. Капилляры выстланы эндотелиоцитами, лежащими на прерывистой базальной мембране.
Иннервация. В иннервации участвуют нервы сосудистых сплетений, нервы мышц и специальные нервные проводники к костному мозгу. Нервы проникают в костный мозг вместе с кровеносными сосудами через костные каналы. Далее покидают их и продолжаются как самостоятельные веточки в паренхиме в пределах ячеек губчатого вещества кости. Они ветвятся на тонкие волоконца, которые либо вновь вступают в контакт с костномозговыми сосудами и оканчиваются на их стенках, либо заканчиваются свободно среди клеток костного мозга.
Возрастные изменения. Красный костный мозг в детском возрасте заполняет эпифизы и диафизы трубчатых костей и находится в губчатом веществе плоских костей. Примерно в 12-18 лет красный костный мозг в диафизах замещается желтым. В старческом возрасте костный мозг (желтый и красный) приобретает слизистую консистенцию и тогда называется желатинозным костным мозгом. Следует отметить, что этот вид костного мозга может встречаться и в более раннем возрасте, например при развитии костей черепа и лица.
Регенерация. Красный костный мозг обладает высокой физиологической и репаративной регенерационной способностью. Источником образования гемопоэтических клеток являются стволовые клетки, находящиеся в тесном взаимодействии с ретикулярной стромальной тканью. Скорость регенерации костного мозга в значительной мере связана с микроокружением и специальными ростстимулирующими факторами гемопоэза.
История исследований костного мозга В 1963 году полномасштабное исследование красного костного мозга провела исследовательская группа кафедры гистологии и эмбриологии Педиатрического факультета РГМУ под руководством М.И.Пекарского.
Паренхима красного костного мозга образована
1) функционально-генетическая классификация (пригодна для всех кроветворных органов):
— первичные или центральные (красный костный мозг; тимус);
— вторичные или периферические (селезенка; ЛУ, миндалины и др.);
2) морфо-функциональная классификация:
— экстралимфатические (тимус, миндалины, а также лимфоидные узелки и предузелки);
— лимфатические (ЛУ, а также лимфоидные бляшки и узелки).
Тимус занимает особое место в системе рециркуляции лимфоцитов (Хэм А., Кормак Д., 1983; Сапин М.Р., Этинген Л.Е., 1996). Наиболее простой вариант:
1) корковое вещество содержит кровеносные капилляры, которые заканчиваются в посткапиллярных венулах с высокими эндотелиоцитами мозгового вещества;
2) отток Т-лимфоцитов происходит из мозгового вещества тимуса через посткапиллярные венулы с высокими эндотелиоцитами.
Более сложный, дискуссионный вариант:
1) лимфоциты поступают в корковое вещество тимуса и уходят из него через капилляры;
2) мозговое вещество тимуса связано с паренхимой вторичных лимфоидных органов через посткапиллярные венулы с высокими эндотелиоцитами.
При этом также возможны варианты соотношения коркового и мозгового вещества тимуса:
1) они не взаимосвязаны (нет перехода лимфоцитов между ними);
2) взаимосвязаны (часть лимфоцитов переходит в мозговое вещество);
3) часть лимфоцитов возникает не в корковом веществе, а в мозговом. Тимус первого варианта близок к ЛУ, во втором варианте это относится к мозговому веществу тимуса, тогда как его корковое вещество напоминает селезенку в части путей поступления лимфоцитов в орган.
Заключение
В современных Международных анатомической и гистологической терминологиях основополагающим признаком объединения совершенно разных очагов кроветворения в единую лимфоидную систему стала их иммунопоэтическая функция, что представляется необоснованным с морфологической и с генетической точек зрения. Такую совокупность указанных органов и структур можно определять только как лимфоидный аппарат (подобная ситуация с эндокринными железами). Тем более, что красный костный мозг, лимфоидные бляшки, узелки и предузелки не являются самостоятельными органами. К собственно лимфоидным органам можно отнести тимус, ЛУ и, возможно, миндалины.
III. Строение костного мозга, методы исследования.
Костный мозг (mielum, medulla ossium).
Миелопоэз протекает в кроветворном красном костном мозге всех костей скелета у детей до 3-4 лет и плоских костей и эпифизах трубчатых костей – у взрослых. Вес красного костного мозга у взрослых 1400 г.
Костный мозг представлен стромой и паренхимой. Строму составляют соединительно-тканные клетки (фиброциты и фибробласты), макрофаги, клетки жировой ткани (адипоциты), эндотелиальные клетки сосудов, остеоциты. Соединительно-тканные клетки костного мозга образуют эластиновые и коллагеновые волокна, которые соединяясь между собой, образуют губчатую структуру в виде сети, в петлях которой располагается костно-мозговая паренхима. Клетки стромы синтезируют активные вещества (гемопоэтины, интерлейкины и др.), необходимые для нормального кроветворения, они создают клеточное микроокружение для нормальной работы клеток-предшественниц. Паренхиму костного мозга составляют клетки-предшественницы гемопоэза, морфологически дифференцированные, делящиеся и созревающие клетки эритроцитарного, гранулоцитарного, моноцитарного, тромбоцитарного рядов.
Кровеносная система костного мозга замкнута соприкосновения паренхимы и циркулирующей крови нет. Сосудистая сеть костного мозга образована центральной артерией кости и проходящими через наружную пластинку кости множественными артериями. Концевые капилляры этих двух систем соединяясь, образуют сеть костно-мозговых синусов.
Зрелые клетки проходят в кровоток через миграционные поры эндотелия стенки синусов. Через костно-мозговой синусовый барьер проходят только зрелые клетки, изменяя форму. При повреждении метастазами злокачественных опухолей, токсинами, лейкозными инфильтратами стенок костно-мозговых синусов, в периферическую кровь попадают незрелые клетки (молодые гранулоциты, нормобласты, осколки ядер мегакариоцитов). Выход клеток костного мозга в периферическую кровь называется миелемией.
Костный мозг кроме основной кроветворной функции участвует в процессах обмена веществ, является центральным органом иммунной системы, депо форменных элементов крови.
Используется два метода:
1) Цитологическое исследование костно-мозгового пунктата;
2) Гистологическое исследование (трепанобиопсия).
Чаще используется цитологическое исследование.
IV. Теория кроветворения: деление клеток на классы, их морфологическая характеристика.
Особое место в учении о кроветворении занимает унитарная теория, созданная А.А. Максимовым. Признанной современной схемой кроветворения является схема, предложенная И.Л. Чертковым и А.И. Воробьевым.
Экспериментально (с помощью новых, так называемых клональных методов) подтверждено существование полипотентной клетки-родоначальницы для всех ростков кроветворения. Эта клетка называется стволовой.
Она оказалась способной:
к самоподдержанию (т.е. поддержанию постоянного уровня себе подобных);
к дифференцировке по всем рядам кроветворения (т.е. превращению клеток вплоть до зрелых, поступающих в периферическую кровь).
В схеме кроветворения различают 6 классов.
II класс – частично дифференцированные полипотентные клетки. Сюда относятся клетки-предшественницы миелопоэза и лимфопоэза.
И это всё клетки, относящиеся к миелопоэзу. Клетка-предшественница лимфопоэза, относящаяся ко II классу, даёт начало В лимфопоэтин чувствительным клеткам и Т лимфопоэтин чувствительным клеткам III класса.
Клетки-предшественницы I, II, III классов морфологически нераспознаваемы, недифференцированные клетки.
VI – зрелые клетки: тромбоциты (пластинки), эритроциты: сегментоядерные нейтрофилы; моноциты; лимфоциты; плазмоциты.
Органы кроветворения и иммунной защиты.
Костный мозг. Тимус. Лимфатические и гемолимфатические узлы. Селезенка
Пользуясь лекциями (на web-странице кафедры размещены презентации и текст лекций), учебниками, дополнительной литературой и другими источниками, студенты должны подготовить такие теоретические вопросы:
1. Общий план строения, функциональное значение и классификация органов кроветворения.
2. Морфологическая характеристика и локализация миелоидной и лимфоидной систем кроветворения.
3. Структурные компоненты костного мозга и их функциональное значение.
4. Возрастные изменения и регенерация костного мозга.
5. Общая характеристика вилочковой железы как центрального органа Т-лимфоцитопоэза.
6. Микроскопическое и субмикроскопическое строение коркового и мозгового вещества дольки вилочковой железы.
7. Возрастная и акцидентальная инволюция вилочковой железы.
8. Понятие о тимико-лимфатическом статусе, его морфологических проявлениях и значениях для организма.
9. Развитие, общий план строения и функциональное значение лимфоидной кроветворной системы.
10. Лимфатические узлы, структурные компоненты и функциональное значение.
11. Корковое вещество лимфатического узла. Лимфатические фолликулы, клеточный состав, их морфофункциональная характеристика.
12. Паракортикальная зона, клеточный состав, их морфофункциональная характеристика.
13. Мозговое вещество лимфатического узла, его структурные компоненты и функция.
14. Строение и значение лимфатических синусов. Роль ретикулоэндотелиальных клеток в защитных реакциях организма.
15. Морфология и функция гемолимфатических узлов.
16. Общий план строения селезенки и ее функциональное значение для организма.
17. Микроскопическое строение белой пульпы селезенки.
18. Тонкое строение красной пульпы селезенки.
19. Особенности кровоснабжения селезенки, структурные и функциональные особенности венозных синусов.
20. Элементы макрофагической системы в органах кроветворения и их роль в защитных реакциях организма.
К системе кроветворения и иммунной защиты принадлежат такие органы, как красный костный мозг, тимус, скопление лимфоидных элементов в стенке пищеварительного канала и дыхательных путей, лимфатические узлы, гемолимфатические узлы, селезенка. Из них первые два считаются центральными, остальные – периферическими органами кроветворения. Функция центральных органов этой системы связана с образованием всех видов форменных элементов крови, обеспечением условий для антигеннезависимого размножения лимфоцитов. В периферических органах иммуногенеза осуществляется специализация под воздействием антигенов эффекторных имунных клеток (Т- и В-лимфоцитов), которые обеспечивают иммунитет – защиту организма от генетически чужого материала, а также элиминация (уничтожение) клеток крови, которые закончили свой жизненный цикл.
Все органы кроветворения в основе своего строения имеют ретикулярную ткань, которая образует каркас и микроокружение для созревающих форменных элементов крови. Кроме размножения клеток крови, в органах кроветворения депонируются кровь и лимфа, осуществляется их очистка от посторонних частиц. Об исключительной важности нормального функционирования этой системы для организма свидетельствует хотя бы тот факт, что два опаснейших и практически неизлечимых патологических состояния – синдром приобретенного иммунного дефицита (СПИД) и злокачественные новообразования, – непосредственно связаны с поражением органов иммунной системы. Отсутствие эффективных методов лечения этих заболеваний свидетельствует о сложности процессов иммунной защиты и тесной взаимосвязи всех органов кроветворения.
Рис. 1. Схематическое изображение локализации органов кроветворения в теле человека.
КРАСНЫЙ КОСТНЫЙ МОЗГ (medulla ossium rubra) – центральный орган кроветворения, в котором содержатся стволовые кроветворные клетки и происходит размножение и дифференциация клеток миелоидного и лимфоидного рядов: образуются эритроциты, тромбоциты, гранулоциты, моноциты, В-лимфоциты и предшественники Т-лимфоцитов. Во взрослом организме красный костный мозг размещен в эпифизах трубчатых костей и в губчатом веществе плоских костей. Общая масса красного костного мозга – 4-5% массы организма, что при массе тела 70 кг составляет 3-3,5 кг
Рис. 2. Схема локализации красного костного мозга: А – в теле человека; Б – в губчатом костном веществе позвонка.
Костный мозг имеет полужидкую консистенцию, на вид он темно-красного цвета. Трабекулы губчатых костей образуют опору для ретикулярной ткани, которая в свою очередь служит каркасом для гемопоэтических клеток, – стволовых, полустволовых, диферонов эритроцитарного, тромбоцитарного, гранулоцитарного, моноцитарного и лимфоцитарного рядов. Для гемопоэтичних клеток характерное формирование островков, в которых размещены клетки того или другого гистогенетического ряда. Процессы пролиферации и созревания клеток наиболее интенсивны возле эндоста. Красный костный мозг хорошо васкуляризован, причем наличие гемокапилляров пористого типа (синусоидов) обеспечивает возможность выхода зрелых клеток крови в кровообращение. Следует заметить, что в нормальных условиях синусоидные гемокапилляры костного мозга проницательные для незрелых клеток крови. Эта выборочная проницательность, очевидно, связанная со спецификой химического состава и цитотопографии углеводных детерминант поверхности зрелых и недостаточно дифференцированных клеток.
Рис. 3. Световая микрофотография красного костного мозга. В центре поля зрения оксифильные костные трабекулы, образующие грубую строму органа. Междутрабекулярное пространство заполнено ретикулярной тканью (нежная строма) а также миелоидной и лимфоидной тканью (паренхима органа). Наиболее интенсивно гемопоэз происходит именно у эндоста костных трабекул, так как остеобласты способны активировать гемопоэз, выделяя различные классы гемопоетинов.
Формирование красного костного мозга начинается на втором месяце эмбрионального развития в ключице эмбриона. На пятом-седьмом месяце эмбриогенеза красный костный мозг функционирует как основной кроветворный орган, причем в этот период в нем преобладают процессы эритропоэза. В детском возрасте красный костный мозг заполняет диафизы и эпифизы трубчатых костей, плоские кости. В 12–18 лет красный костный мозг в диафизах трубчатых костей замещается на желтый костный мозг. В состав последнего входят адипоциты. В норме желтый костный мозг не несет функций гемопоэза, однако при массивной кровопотере в нем могут появляться центры миелоидного кроветворения. В старческом возрасте красный и желтый костный мозг приобретают гелеобразную консистенцию и называются желатинозным костным мозгом.
Рис. 4. Схематическое воспроизведение части красного костного мозга
Рис. 5. Схема эритропоэтического островка. В центре находится макрофаг, создающий благоприятное микроокружение для созревающих эритробластов и их предшественников.
Рис. 7. Ретикулоциты с остатками гранулярной эндоплазматической сети могут выходить в кровеносное русло из красного костного мозга. Световая микрофотография мазка крови. Окраска по Романовскому-Гимзе.
Рис. 9. Световая микрофотография фрагмента красного костного мозга. Окраска гематоксилин-эозином. В центре поля зрения – мегакариоцит – гигантская многоядерная клетка – продуцент тромбоцитов.
Кровоснабжение костного мозга осуществляется сосудами, которые входят через надкостницу в специальные отверстия в компактной кости. В костной ткани эти артерии разветвляются на восходящие и нисходящие ветви, из которых в радиальном направлении отходят артериолы. Далее они разветвляются в узкие капилляры (4-10 мкм), а затем в эндосте трансформируются в пазухи – синусоидальные капилляры (20-30 мкм в диаметре). Из них кровь собирается в центральные венулы. Гидростатическое давление в капиллярных пазухах выше, чем в венулах, поэтому синусы имеют постоянно зияющие щели в эндотелиальном слое. Пористая базальная мембрана и не сплошной слой адвентициальных клеток вокруг пазух создают благоприятные условия для миграции клеток из красного костного мозга в кровь. Меньшее количество крови переходит от надкостницы в остеонные каналы, а оттуда через эндост в пазухи. Находясь в контакте с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения.
На кровеносные сосуды приходится до 50 % массы костного мозга и 30 % из них – только на синусоиды. В костном мозге различных костей артерии имеют хорошо развитую мышечную и адвентициальную оболочки, многочисленные венулы с тонкой стенкой. Кстати, как правило, артерии и вены проходят отдельно. Есть два типа капилляров в костном мозге: тонкие соматического типа – 4-10 мкм и широкие типичные синусоиды 20-50 мкм в диаметре. Тонкие капилляры выполняют питательную функцию, в то время как большие являются местом проникновения зрелых клеток крови в периферийный кровоток и местом созревания эритроцитов.
Иннервация. Костный мозг иннервируется от сплетений ближайших кровеносных сосудов, нервов и мышц. Нервы входят в костный мозг с кровеносными сосудами через каналы кости. Позже в костномозговой паренхиме губчатой кости они оставляют сопутствующие сосуды и разветвляются в тонкие волокна, свободно лежащие между клетками костного мозга.
ТИМУС (thymus) – центральный орган иммуногенеза, в котором происходит размножение и созревание (антигеннезависимая дифференциация) Т-лимфоцитов. В тимусе продуцируются тимозин, тимулин, тимопоэтин и другие регуляторные пептиды, которые обеспечивают пролиферацию и созревание Т-лимфоцитов в центральных и периферических органах иммуногенеза, а также ряд других биологически активных веществ: инсулиноподобный фактор (снижает уровень сахара в крови), кальцитониноподобный фактор (снижает уровень кальция в крови), фактор роста (обеспечивает рост тела).
Тимус размещен за грудиной. Его масса у взрослого человека составляет 10. 30 г, у новорожденных детей – около 12. 14 г. Форма тимуса полигональная, для нее характерна значительная индивидуальная и возрастная изменчивость. В 18-летнем возрасте размеры тимуса около 19х7х2 см. Внешне тимус покрыт соединительнотканной капсулой, от которой внутрь органа отходят перегородки, разделяющие его на дольки. Соединительная ткань капсулы тимуса ограничена от его паренхимы базальной мембраной пористого типа, которая в местах врастания кровеносных сосудов формирует характерные каналы, которые идут вглубь органа.
Дольки тимуса являются структурной и функциональной единицей органа. Основой дольки является каркас из так называемых эпителиоретикулоцитов – особенных эпителиальных клеток звездчатой формы, которые контактируют своими отростками, образуя сетчатый симпласт. Промежутки между эпителиоретикулоцитами заполнены преимущественно Т-лимфоцитами, в меньшей степени – макрофагами. Незначительную часть среди клеточных элементов тимуса составляют фибробласты, миофибробласты, а также тканевые базофилы. Центральный участок дольки тимуса, который на гистологических препаратах окрашивается светлее от периферии, имеет название мозгового вещества; темную периферию дольки называют корковым веществом.
Рис. 10. Микрофотография фрагмента тимуса. В каждой дольке видно центральную светлую зону – мозговое вещество и периферийную темную, интенсивно базофильную – корковое вещество. Между дольками находятся септы – соединительнотканные перегородки. Окраска гематоксилин-эозином.
Рис. 11. Микрофотография коркового вещества тимуса. Стрелками показаны ядра стромальных клеток – эпителиоретикулоцитов. Окраска гематоксилином-эозином.
В корковом веществе дольки тимуса компактно размещены малые и средние лимфоциты в окружении макрофагов (в том числе их разновидности, которая имеет название дендритных клеток) и эпителиоретикулоцитов, а также Т-лимфобласты, причем последние локализуются преимущественно в субкапсулярной зоне. Эпителиоретикулоциты, макрофаги и дендритные клетки субкапсулярной зоны тимуса часто называют тимусными клетками-няньками, поскольку они создают микроокружение и необходимые условия для созревания Т-лимфоцитов (тимоцитов). В корковое вещество тимуса из красного костного мозга переносятся предшественники Т-лимфоцитов. Здесь происходит их пролиферация под действием тимозина, продуцирующийся эпителиоретикулоцитами, и выборочный фагоцитоз части новообразованных клеток макрофагами. Отобранные (нефагоцитированные) Т-лимфоциты мигрируют в мозговое вещество, откуда могут поступать в периферическое кровообращение.
Мозговое вещество дольки тимуса образовано малыми, средними и большими Т-лимфоцитами, которые также окружены эпителиоретикулоцитами и макрофагами, однако размещенные менее компактно по сравнению с корковым веществом. Лимфоциты мозгового вещества являют собой рециркулирующий пул клеток, которые могут попадать в кровообращение и возвращаться обратно в тимус. Характерным морфологическим признаком тимуса является наличие в мозговом веществе особенных концентрических наслоений эпителиальных клеток, которые имеют название тимусных телец Гассаля. Они образуются при дегенерации и взаимном наслоении звездчатых эпителиоретикулоцитов мозгового вещества. Тельца Гассаля окрашиваются оксифильно, в цитоплазме образующих их клеток, находят гранулы кератина, толстые пучки фибрилл и большие вакуоли. В центре тимусных телец размещен оксифильный клеточный детрит. Существует взаимосвязь между появлением телец Гассаля и приобретением Т-лимфоцитами иммунной компетентности.
Рис. 12. Световая микрофотография мозгового вещества дольки тимуса со сформированным тельцем Гассаля. В центре эпителиального тельца видно клеточный детрит, окруженный концентрически напластованными эпителиоретикулярными клетками. Окраска гематоксилин-эозином.
Рис. 13. Схема миграции предшественников эффекторных форм Т- лимфоцитов.
Корковое и мозговое вещества долек тимуса имеют особенности строения микроциркуляторного русла. В частности, лимфоциты коркового вещества отграничены от просвета гемокапилляров так называемым гематотимусным барьером. Он образован сплошным слоем размещенных на базальной мембране эпителиоретикулоцитов, что сопровождают все сосуды микроциркуляторного русла и ограничивают перикапиллярное пространство, а также стенкой гемокапилляров. Гематотимусный барьер ограничивает доступ избыточному количеству антигенов с сосудистого русла к лимфоцитам коркового вещества. Он непроницаем для тех лимфоцитов тимуса, которые имеют циторецепторы к собственным антигенам организма, что предупреждает развитие аутоимунных реакций (повреждение собственных клеток и тканей организма). В мозговом веществе гематотимусный барьер отсутствует, что создает условия для рециркуляции Т-лимфоцитов. Следует отметить, что в норме выход Т-лимфоцитов из коркового и мозгового веществ тимуса в периферийное кровяное русло осуществляется изолировано.
Рис. 14. Световая микроскопия тимуса: А – общий план строения долек Б – фрагмент дольки тимуса ребенка со сформированным тельцем Гассаля в мозговые веществе.
Тимус у человека формируется на пятой неделе эмбриогенеза в виде утолщения эпителия третей–четвертой пар жаберных карманов. В конце второго месяца эпителиальную строму тимуса заселяют первые лимфоциты. На третьем месяце появляются дольки, среди которых можно различить корковое и мозговое вещества, становятся заметными тельца Гассаля. Максимальной массы орган достигает в раннем детском возрасте.
На протяжении всей жизни человека в тимусе происходят изменения, которые получили название возрастной инволюции. Последняя заключается в постепенном замещении паренхиматозных элементов тимуса жировой и рыхлой соединительной тканью, обогащении тельцами Гассаля при почти неизменной общей массе органа. В возрастной инволюции тимуса различают четыре фазы: быструю (до 10 лет), медленную (в промежутке с 10 до 25 лет), ускоренную (от 25 до 40 лет) и замедленную (после 40 лет). Скорость возрастной инволюции тимуса в значительной мере определяется гормональным статусом организма. В старческом возрасте тимус полностью замещается жировой тканью и превращается в жировое тело.
Рис. 15. Световая микрофотография тимуса мужчины 40 лет. Окраска гематоксилин-эозином. Вследствие возрастной инволюции произошло замещение паренхиматозных и стромальных элементов органа белой жировой тканью.
Отсутствие возрастной инволюции тимуса – это проявление тяжелой патологии, которая имеет название тимико-лимфатического статуса. Конечно, это состояние сопровождается недостаточностью глюкокортикоидной функции коры надпочечников, разрастанием лимфоидной ткани в органах. При тимико-лимфатическом статусе резко падает сопротивляемость организма к инфекциям, интоксикациям, растет угроза возникновения злокачественных новообразований.
При действии на организм неблагоприятных факторов – травм, голода, интоксикаций, инфекций – имеет место так называемая акцидентальная инволюция тимуса. При этом наблюдается массовая гибель лимфоцитов, их выселение в периферийные органы иммуногенеза, пролиферация и набухание эпителиоретикулоцитов, в результате чего исчезает разница между корковым и мозговым веществом долек тимуса. Акцидентальная инволюция тимуса является морфологическим проявлением защитных реакций организма.
ЛИМФОИДНАЯ ТКАНЬ СЛИЗИСТОЙ ОБОЛОЧКИ
Слизистая оболочка ЖКТ, воздухоносных и мочевыделительных путей содержит значительное количество ретикулиновых волокон, одного из элементов поддерживающего каркаса органов кроветворения. Здесь, как правило, скапливаются лимфоциты, зачастую формирующие лимфатические фолликулы. Типичным примером лимфоидной ткани в слизистой оболочке являются пейеровы бляшки. В них присутствуют венулы с высоким эндотелием, через стенку которых в бляшку поступают лимфоциты. Бляшка имеет выносящие, но (в отличие от лимфатического узла) не имеет приносящих лимфатических сосудов. Антиген из просвета кишки «подаётся» в бляшку при помощи М-клеток. Собственный слой слизистой оболочки содержит дендритные клетки, отростки которых проникают в эпителий. Они так же, как и М-клетки, взаимодействуют с бактериальной микрофлорой.
Поверхность слизистой оболочки в дыхательной и пищеварительной системах защищена слизью, дефензинами и секреторным IgA. Транспорт, процессинг и представление антигена осуществляются при тесном взаимодействии организованной лимфоидной ткани и ассоциированного с фолликулами эпителия. Периферия лимфатических фолликулов в слизистой оболочке содержат большое количество T–лимфоцитов. В фолликулах присутствуют также B–клетки, дендритные клетки и венулы с высоким эндотелием. В кишке эндотелий подобных венул экспрессирует слизистый адрессин MadCAM-1, который распознаётся клетками, несущими рецептор хоминга a4b7 интегрин. Молекулу MadCAM-1 распознают также неактивированные лимфоциты, экспрессирующие L-селектин. В пейеровых бляшках каждый фолликул отделён от эпителия субэпителиальной куполообразной зоной, богатой Т-, B-лимфоцитами и дендритными клетками. Ассоциированный с фолликулами эпителий содержит М-клетки, которые транспортируют чужеродные макромолекулы и микроорганизмы к антигенпредставляющим клеткам, расположенным по другую сторону эпителиального барьера.
М-клетка — типичная эпителиальная клетка с полярной дифференцировкой, формирующая плотные контакты. Отличительной её особенностью является наличие расположенного в базолатеральной части инвагинированного субдомена, который увеличивает поверхность клетки и образует интраэпителиальный карман. С плазмолеммой этого кармана взаимодействуют интраэпителиальные лимфоциты при участии молекул адгезии. Мембрана апикальной части клетки не участвует в формировании всасывательной каёмки, имеет нерегулярные микроворсинки и микроскладки и приспособлена для прикрепления чужеродных молекул, частиц и микроорганизмов. Здесь же присутствуют области, участвующие в клатрин-опосредованном эндоцитозе окружённых лигандом частиц, молекул адгезии и вирусов. Апикальная часть клетки не покрыта гликокаликсом и лишена интегральных мембранных гидролитических ферментов. Карман, образованный М-клеткой, содержит В- и T–лимфоциты и реже дендритные клетки. Из T–клеток здесь в основном находятся T–клеток памяти. Среди присутствующих в кармане B–лимфоцитов неактивированные B–клетки и B–клетки памяти, которые могут происходить из клеток, лежащих вне фолликулов.
Рис. 16. Роль М-клеток в трансэпителиальном переносе антигенов.
Ассоциированный с фолликулами эпителий покрыт толстым гликокаликсом, который отличается от гликокаликса соседних энтероцитов. Специфический характер гликозилирования его молекул, связанный с особой экспрессией гликозилтрансферазы, важен для узнавания и адгезии микроорганизмов. Гликокаликс содержит меньшее количество связанных с мембраной гидролаз, участвующих в процессе пищеварения. Ассоциированный с фолликулами эпителий продуцирует меньше слизи и в криптах содержит меньшее количество продуцирующих дефензин и лизоцим клеток Панета. Этот эпителий лишён рецепторов Ig и неспособен транспортировать IgA из стенки кишки в её просвет. Всё это указывает на то, что ассоциированный с фолликулами эпителий специализирован для осуществления наилучшего контакта с антигенами, в том числе патогенами, находящимися на поверхности слизистой оболочки. В случае ассоциированного с фолликулами эпителия в подлежащей соединительной ткани собственного слоя слизистой оболочки отсутствуют миофибробласты, которые образуют практически сплошной слой под обычным эпителием ворсинок. Базальная мембрана здесь содержит большее количество пор и отверстий для усиленной миграции клеток в эпителий и из него.
Субэпителиальная куполообразная зона расположена тотчас под ассоциированным с фолликулами эпителием и представлена густой сетью дендритных клеток. Все эти дендритные клетки являются неактивированными. Полагают, что они захватывают большинство антигенов, транспортируемых М-клетками через ассоциированный с фолликулами эпителий.
Локализация пейеровых бляшек в строго определённых участках пищеварительного тракта детерминирована генетически и прослеживается в плодном периоде. Сигнальными молекулами в морфогенезе пейеровых бляшек и других лимфоидных структур в слизистой оболочке служат рецепторы ИЛ7, представители семейства фактора некроза опухоли (TNF) и семейства его рецепторов.
В современной иммунологии лимфоидную ткань слизистых оболочек и кожи рассматривают как неинкапсулированную лимфоидную ткань. К ней относятся лимфоидная ткань слизистых оболочек, субпопуляция лимфоцитов печени и лимфоидная подсистема кожи.
⃰ Лимфоидная ткань, ассоциированная с ЖКТ (GALT — gut–associated lymphoid tissue) — миндалины, аппендикс, пейеровы бляшки, а также субпопуляция внутриэпителиальных лимфоцитов слизистой оболочки ЖКТ.
⃰ Лимфоидная ткань, ассоциированная с бронхами и бронхиолами (BALT — bronchus–associated lymphoid tissue), а также внутриэпителиальные лимфоциты слизистой оболочки дыхательной системы.
⃰ Лимфоидная ткань, ассоциированная с женскими половыми путями (VALT — vulvovaginal–associated lymphoid tissue), а также внутриэпителиальные лимфоциты слизистой оболочки.
⃰ Лимфоидная ткань, ассоциированная с носоглоткой (NALT — nose–associated lymphoid tissue), а также внутриэпителиальные лимфоциты слизистой оболочки.
√ Субпопуляция лимфоцитов печени, которая в качестве лимфоидного барьера «обслуживает» кровь воротной вены, несущей все всосавшиеся в кишечнике вещества.
√ Лимфоидная подсистема кожи — диссеминированные внутриэпителиальные лимфоциты и регионарные лимфатические узлы и сосуды лимфодренажа.