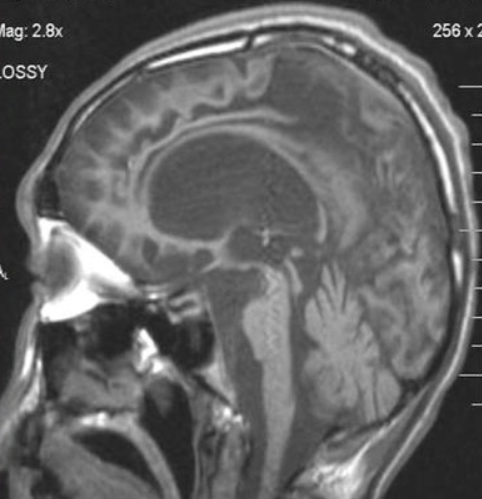
Признаки атрофии мозга на мрт
а) Определение:
• ↓ общего объема головного мозга с возрастом:
о Проявляется в относительном расширении ликворных пространств
1. Общие характеристики возрастных изменений головного мозга:
• Лучший диагностический критерий:
о «Благоприятное течение возрастных изменений головного мозга»:
— Тонкий перивентрикулярный гиперинтенсивный ободок
— Небольшое число гиперинтенсивных очагов в белом веществе (ГОБВ) или их отсутствие
— Легкое уменьшение отдельных отделов мозжечка
• Локализация:
о Преобладание избирательной атрофии белого вещества (БВ), но не серого вещества (СВ)
о Полосатое тело (преимущественно хвостатые ядра, скорлупа)
• Размеры:
о Уменьшение общего объема головного мозга
о Абсолютные размеры полосатых тел
— Линейный характер уменьшения размеров хвостатых ядер с течением возраста
— Размеры скорлупы относительно постоянны
• Морфология:
о ↓ объема ткани головного мозга, ↑ объем ЦСЖ:
— Отражает уменьшение общего объема БВ > ГОБВ
— Округленный внешний вид расширенных желудочков, расширение борозд
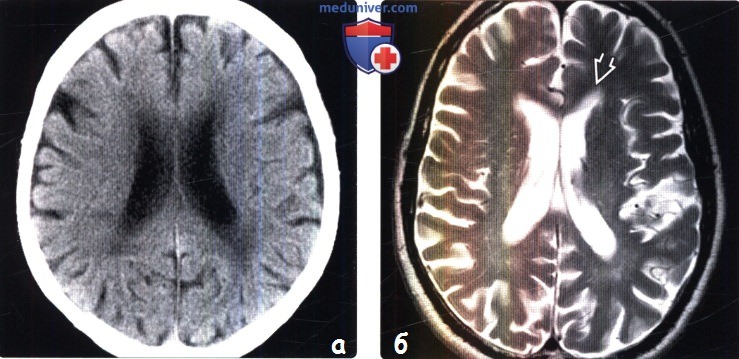
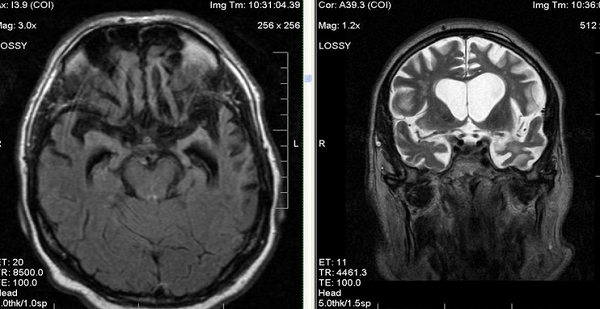
(б) МРТ 3Т,Т2-ВИ, аксиальный срез: у пациента 76 лет визуализируется легкое повышение интенсивности сигнала от перивентрикулярного белого веществам, а также легкие вентрикуломегалия и расширение борозд.
2. КТ признаки возрастных изменений головного мозга:
• Бесконтрастная КТ:
о Расширение желудочков, борозд
о Перивентрикулярные фрагментарные гиподенсные участки
о ± симметричные точечные кальцификаты в бледных шарах (БШ)
о ± кальцификация сосудов криволинейной формы
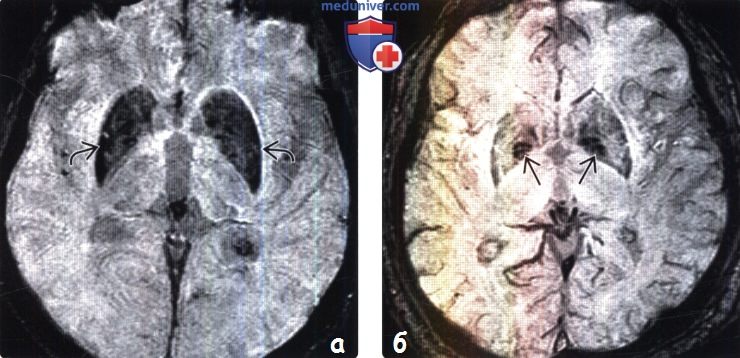
(б) MPT, Т2*5WI, аксиальный срез: визуализируются горизонтальные линейные «волны» минерализации в бледных шарах, что является нормальной находкой в головном мозге с возрастными изменениями.
4. Радионуклидная диагностика:
• ПЭТ:
о Часто отмечаются метаболические изменения:
— Глобальные, регионарные изменения CBF
о Постепенное ↓ регионарного мозгового кровотока (CBF) в СВ, БВ:
— Главным образом, в лобных долях
о Разность уровня метаболизма в коре по направлению от передних отделов полушарий к задним вследствие возрастных изменений
о Относительная скорость метаболизма глюкозы (rGMR), измеренная при ПЭТ с ФДГ:
— С возрастом наблюдается ↓ rGMR в скорлупе и ее ↓ в хвостатых ядрах
о ↓ пре-/постсинаптических допаминовых маркеров в БГ
• При ОФЭКТ с Тс-99m-ГМПАО, ингаляции Хе-133 наблюдается регионарное, а также глобальное снижение CBF
5. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ с FLAIR, ДВИ, Т2* GRE/SWI
в) Дифференциальная диагностика возрастных изменений головного мозга:
1. Легкие когнитивные нарушения:
• «Перекрытие» признаков с нормальной картиной при стандартных методиках визуализации
• ↓ пика NAA
2. Болезнь Альцгеймера:
• Атрофия теменных и височных отделов коры
• Выраженное снижение объема гиппокампов, энторинальной коры
• ↓ пика NAA, ↑ пика миоинозитола (ml)
3. Спорадическая субкортикальная артериосклеротическая энцефалопатия:
• Множественные ГОБВ («перекрытие» с нормальной картиной)
• Множественные лакунарные инфаркты
4. Сосудистая деменция:
• Гиперинтенсивные на Т2-ВИ поражения и локальная атрофия, отражающие хронические инфаркты
5. Лобно-височная дегенерация:
• Ассиметричная атрофия лобных, передних отделов височных долей
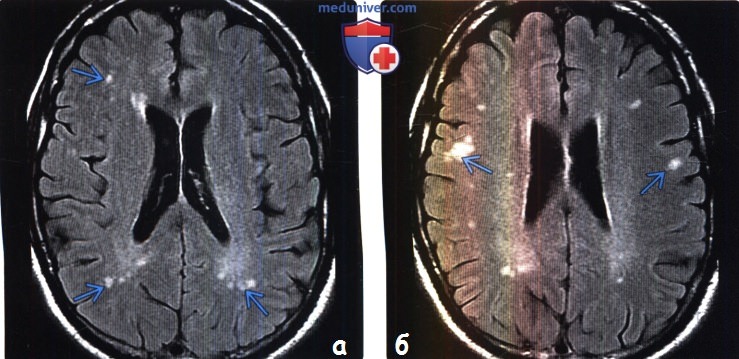
(б) MPT, FAIR, аксиальный срез: у этого же пациента визуализируются другие субкортикальные гиперинтенсивные очаги.
1. Общие характеристики возрастных изменений головного мозга:
• Этиология:
о Ранее принятая концепция возрастных изменений: значимое уменьшение количества нейронов с возрастом
о Новая: преобладание нейроанатомических изменений:
— Изменения БВ, потеря нейронов в субкортикальных отделах
— Уменьшение размеров клеток > уменьшение количества клеток
о Скорее характерна дисфункция нейронов, чем потеря нейро-нов/синапсов:
— ↓ жизнеспособности или функций нейронов, связанное с ускорением деградации мембран и/или ↑ количества клеток глии
— Потеря синапсов и синаптический прунинг имеет скорее локальный (в отдельных областях), чем глобальный характер
о Согласно некоторым исследованиям накопление нейрофибриллярных клубков (НФК) может обусловливать снижение памяти с возрастом
• Генетика:
о Отчетливое влияние на процессы возрастных изменений головного мозга
о Аполипопротеин Е (АроЕ) и шесть новых связанных с риском однонуклеотидных полиморфизмов (ОНП) в локусе 17q25 имеют связь с развитием патологических изменений головного мозга с возрастом
2. Макроскопические и хирургические особенности:
• Расширение борозд, пропорциональное расширение желудочков
• Незначительное истончение плащевых отделов полушарий, преимущественные изменения со стороны субкортикального БВ
д) Клиническая картина:
1. Проявления возрастных изменений головного мозга:
• Наиболее частые признаки/симптомы:
о Нормальные когнитивные функции
о Легкие когнитивные нарушения коррелируют с ↑ риска развития болезни Альцгеймера
2. Демография:
• Возраст:
о > 60 лет
• Пол:
о Различия в размерах полосатого тела:
— Относительно постоянные размеры в течение всей жизни у мужчин
— Вариабельные в зависимости от возраста изменения размеров у женщин: меньшие размеры у женщин в возрасте 50-70 лет, чем у мужчин
• Эпидемиология
о ГОБВ коррелируют с возрастом, бессимптомным инсультом, артериальной гипертензией, женским полом
3. Течение и прогноз:
• Прогрессирующее ↑ объема паренхимы, ↓ ликворных пространств
• Прогрессирующее ↑ количества ГОБВ с возрастом
е) Диагностическая памятка:
1. Обратите внимание:
• Изменения полосатых тел могут быть связаны с возрастным снижением когнитивных функций:
о ↓ объема, функциональной активности с возрастом
2. Советы по интерпретации изображений:
• Широкий спектр «нормы» при диагностической визуализации у пожилых людей
• Предсказание когнитивных функций по данным КТ/МРТ невозможно
ж) Список литературы:
1. Xekardaki A et al: Neuropathological changes in aging brain. Adv Exp Med Biol. 821:11-7, 2015
2. van Velsen EF et al: Brain cortical thickness in the general elderly population: the Rotterdam Scan Study. Neurosci Lett. 550:189-94, 2013
3. Poels MM et al: Arterial stiffness and cerebral small vessel disease: the Rotterdam Scan Study. Stroke. 43(10):2637-42, 2012
4. Ikram MAet al: The Rotterdam Scan Study: design and update up to 2012. Eur J Epidemiol. 26(10):811-24, 2011
5. Poels MM et al: Incidence of cerebral microbleeds in the general population: the Rotterdam Scan Study. Stroke. 42(3):65б—61, 2011
Редактор: Искандер Милевски. Дата публикации: 3.5.2019
Атрофия головного мозга на МРТ
Магнитно-резонансная томография признана одним из наиболее информативных нейровизуализационных методов исследования. В ходе процедуры получают детальные послойные снимки головного мозга, позволяющие оценить соответствие органа нормам.
МРТ актуальна при диагностике посттравматических состояний, воспалительных, опухолевых, нейродегенеративных изменений. Одно из самых тяжелых нарушений, выявляемых с помощью томографии — атрофия головного мозга. Это хроническое прогрессирующее заболевание, сопровождающееся гибелью нейронов, уменьшением объема и плотности структур головного мозга.
Атрофия лобных и височных долей на МР-сканах
В основе патологии лежат органические изменения в нервной ткани. Прогрессирование атрофии ведет к снижению функциональных возможностей ЦНС. Фактически это означает постепенное угасание работы (инволюцию) мозга вплоть до остановки жизненно важных процессов. Прогнозы неблагоприятные, так как изменения необратимы. Перспективы зависят от этиологии, формы, скорости прогрессирования болезни и качества оказываемой медицинской помощи.
Посредством МР-томографии можно выявить и определить локализацию указанных процессов на ранних этапах развития.
Признаки атрофии головного мозга
Патология может быть первичной и вторичной. Классификация обусловлена причинами развития заболевания. При первичной атрофии выявляют аномалии головного мозга и генетические нарушения. Отклонения могут манифестировать в любом возрасте, часто быстро прогрессируют, сложно поддаются коррекции.
Левосторонняя инволюция ткани головного мозга
Вторичная атрофия связана с воздействием внешних и внутренних неблагоприятных факторов. Инволюция нервной ткани может быть следствием черепно-мозговых травм, патологий сосудов, метаболических нарушений, вредных привычек, воздействия радиации и т.д. В данном случае устранение причины может способствовать замедлению развития заболевания. Правильная медикаментозная терапия способна обеспечить стабильное удовлетворительное состояние и качество жизни пациента на долгие годы.
Клинические проявления атрофии включают расстройства высшей нервной деятельности, нарушения синхронизации функций различных частей организма.
Симптомами заболевания могут быть:
проблемы со скелетной мускулатурой (от снижения тонуса до полной утраты способности двигаться);
снижение слуха и зрения вплоть до полной утраты;
речевые нарушения (от обеднения словарного запаса до невозможности изъясняться);
снижение или утрата обоняния;
изменение чувствительности разных частей тела;
нарушение координации движений;
потеря пространственной ориентации;
изменение поведения (от раздражительности до паранойи);
эмоциональная нестабильность (от чрезмерного возбуждения до полной аутизации).
Проблема диагностики атрофии головного мозга заключается в отсутствии или слабом проявлении симптомов на ранних этапах развития заболевания. Выделяют следующие стадии патологии:
Первая. Органические изменения в мозге минимальны, но уже присутствует слабая неврологическая симптоматика. Отмечают снижение способности к концентрации внимания, расстройство памяти, эмоциональную лабильность.
Вторая. Появляются нарушения слуха, зрения, речи. Существенно меняется поведение человека, возможны нелогичные поступки, которые сам больной не может объяснить или сразу забывает.
Как выглядит атрофия головного мозга на МРТ?
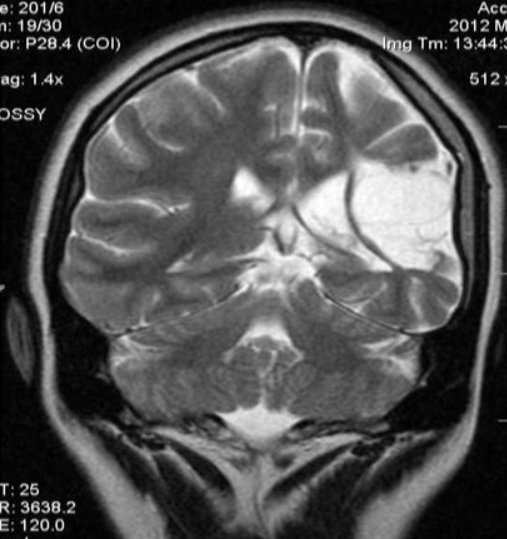
Диффузная атрофия головного мозга с вентрикуломегалией
Явление дифференцируют с истинной гидроцефалией. Главный МРТ-признак атрофии головного мозга — пропорциональное расширение внутренних и наружных ликворных церебральных пространств, что указывает на уменьшение объема структур органа. Выраженность изменений оценивают с помощью церебро-вентрикулярного индекса (ЦВИ Эванса). Учитывают и другие отклонения в ткани головного мозга.
Симптомы патологии на МРТ-снимках:
увеличение ЦВИ Эванса;
расширение субарахноидальных борозд и щелей;
снижение плотности мозговой ткани;
дистрофия белого вещества;
уменьшение долей мозга в размерах.
В зависимости от локализации патологических изменений и степени вовлеченности структур атрофия может быть:
кортикальной (главный признак — инволюция коры на уровне лобных и височных долей);
мультисистемной или диффузной (очаги обнаруживаются сразу на нескольких участках);
генерализованной (изменения происходят во всех отделах органа).
Признаки атрофии мозга на мрт
ФГБУ «Научный центр неврологии» РАН, Москва
ФГБНУ «Научный центр неврологии», Москва
Научный центр неврологии РАМН, Москва
Атрофия центральной нервной системы при рассеянном склерозе: данные МРТ-морфометрии
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2014;114(10-2): 50-56
Кротенкова И. А., Брюхов В. В., Переседова А. В., Кротенкова М. В. Атрофия центральной нервной системы при рассеянном склерозе: данные МРТ-морфометрии. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2014;114(10-2):50-56.
Krotenkova I A, Briukhov V V, Peresedova A V, Krotenkova M V. Atrophy of the central nervous system in multiple sclerosis: MRI-morphometry results. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2014;114(10-2):50-56.
ФГБУ «Научный центр неврологии» РАН, Москва
В настоящее время большое внимание при рассеянном склерозе (РС) уделяется нейродегенеративному компоненту, для оценки которого применяют метод воксельной МРТ-морфометрии. Представлен обзор литературы, которая свидетельствует о том, что атрофия головного мозга начинается на самых ранних стадиях заболевания и развивается при различных типах его течения, в среднем втрое превышая норму. Атрофия белого вещества (БВ) затрагивает практически все отделы головного мозга, но выражена в меньшей степени по сравнению с атрофией серого вещества (СВ). Выявлены определенные паттерны поражения коры и подкорковых структур у пациентов с разными типами течения РС, более выраженные при прогрессирующих типах. Отмечено, что атрофия подкорковых структур связана как с изменениями БВ, так и с атрофией коры. Показаны корреляции между атрофией СВ и общим объемом очагов, визуализируемых в МРТ-режиме Т2-ВИ, когнитивными нарушениями и степенью инвалидизации пациентов. Кроме того, у пациентов с РС выявляется атрофия спинного мозга, которая также коррелирует с тяжестью клинической симптоматики. Однако последовательность развития атрофических изменений при РС требует уточнения, необходима дальнейшая разработка МРТ-предикторов атрофии в отношении мониторирования течения болезни.
ФГБУ «Научный центр неврологии» РАН, Москва
ФГБНУ «Научный центр неврологии», Москва
Научный центр неврологии РАМН, Москва
До недавнего времени рассеянный склероз (РС) традиционно расценивался как первично демиелинизирующее заболевание. Однако в настоящее время общепринятым является мнение, что в его патогенезе участвуют как иммуно-воспалительные, так и нейродегенеративные компоненты, при этом именно баланс между активностью воспаления, прогрессирующей дегенерацией и репаративными механизмами и определяет клинические проявления РС на каждом конкретном этапе [1].
Атрофия головного мозга начинается на самых ранних стадиях заболевания и развивается как при ремиттирующем, так и прогрессирующем типах течения РС. Причем у всех пациентов с РС (без разделения на типы течения) объем мозга уменьшается в среднем на 0,5-1,3% в год, что втрое превышает нормальное старение мозга (0,1-0,4%) [9]. Показана связь степени атрофии с типом течения, стадией заболевания, генетическими и токсическими факторами. Было выявлено, что у пациентов с различными типами течения РС и клинически изолированным синдромом (КИС) снижение объема головного мозга в целом на 5,7% больше по сравнению с контролем, причем у пациентов с вторично-прогрессирующим типом течения РС (ВПРС) оно значительно выше, чем при ремиттирующем РС (РРС).
У пациентов с аполипопротеином Е-е4 в генотипе ежегодное уменьшение объема мозга в 4 раза выше, чем у пациентов с его отсутствием. Однако согласно другим исследованиям, генотип с наличием аполипопротеина Е-е4 не влияет на степень атрофии [10]. Подверженность токсическому воздействию, например табачному дыму, также повышает степень атрофии.
В настоящее время доказано, что атрофические процессы в ЦНС при РС обусловлены не только потерей миелина, но и нейродегенеративным процессом с потерей аксонов, нейронов, что отражается в уменьшении объема коры и подкорковых структур. В связи с этим при оценке атрофического процесса у больных РС с помощью метода воксельной морфометрии выделяются следующие составляющие: атрофия БВ, коры головного мозга и подкорковых структур.
Атрофия БВ
Однако согласно другим работам, соотношение между степенью очагового повреждения БВ и атрофией СВ довольно незначительна, так как к уменьшению его объема ведут и другие процессы.
Атрофия коры головного мозга
У пациентов с РС (без разделения по типам течения) отмечается диффузная и локальная атрофия коры головного мозга. Средняя толщина коры у пациентов с РС составляет 2,3 мм по сравнению с 2,48 мм у здоровых людей. Выявляется преимущественная атрофия коры лобных (2,37 мм по сравнению с 2,73 мм в группе контроля) и теменных долей (2,65 по сравнению с 2,95 мм) даже на ранних стадиях заболевания. У пациентов с большой длительностью заболевания преимущественно атрофируется моторная кора (2,35 мм по сравнению с 2,74 мм в норме) [12].
В ходе метаанализа у пациентов с различными типами течения РС, без разделения на группы, была выявлена преимущественная атрофия коры пре- и постцентральных извилин (более выраженная в левом полушарии), левой средней лобной извилины, нижней теменной дольки правого полушария большого мозга, поясных извилин, преимущественно правой задней поясной и левой парагиппокампальной извилин [17].
Атрофия подкоркового СВ
Согласно последним данным, атрофия таламуса развивается раньше, чем атрофия коры, что было продемонстрировано в исследовании пациентов с РРС и ППРС при динамическом наблюдении [18, 19]. Атрофия таламуса отмечается при всех типах течения РС, в наибольшей степени при ВПРС, что, вероятно, связано с длительностью заболевания.
В работе A. Cifelli и соавт. [20] было показано, что по сравнению с группой контроля у пациентов с ВПРС объем таламуса уменьшился на 17%, а поперечный размер III желудочка возрос вдвое, причем была выявлена четкая обратно пропорциональная зависимость между их объемами. Вышеописанные МРТ-данные подтверждаются гистологическими исследованиями: выявлено сокращение числа нейронов в медиальном заднем таламическом ядре и уменьшение общего объема таламуса в среднем на 22%. В целом потеря нейронов головного мозга оценивалась в 30-35%. Сходные данные были получены у пациентов с РРС в ходе оценки концентрации N-ацетиласпартата (NAA) в таламусе, и именно его снижение коррелировало с атрофией таламуса и продолжительностью заболевания.
В ходе вышеупомянутого метаанализа у пациентов с РРС и КИС зона наибольшей атрофии была в правом таламусе, а также отмечалось билатеральное вовлечение подкорковых структур, включая левый таламус.
Согласно одним данным [21, 22], у пациентов с КИС не обнаруживалось зон значительного снижения объема СВ, в частности таламуса, по сравнению с контролем. Однако, согласно другим исследованиям с использованием воксельной МРТ-морфометрии [23, 24] и режима Т1-ВИ с применением импульса переноса намагниченности, отмечалась атрофия таламуса [25]. Расхождение данных может быть связано с тем, что режим Т1-ВИ с применением импульса переноса намагниченности обладает большей чувствительностью по отношению к изменениям СВ, которые предшествуют атрофии. Противоречивые результаты вышеописанных исследований могли быть получены также из-за различных методик, которые применялись для измерения атрофии. По данным метаанализа было выявлено, что у пациентов с РРС и КИС правый таламус является наиболее пораженной зоной. Когда из списка всех работ исключили исследования, в которых принимали участие пациенты с КИС, было выявлено незначительное изменение паттернов распределения атрофии СВ. Пик атрофии при этом сместился в левый таламус.
У пациентов с ВПРС по сравнению с РРС наблюдалось значительное снижение объема некоторых подкорковых структур (таламус, хвостатые ядра), верхних и нижних холмиков крыши четверохолмия. По сравнению с пациентами с ППРС, при ВПРС отмечалась более выраженная атрофия таламуса с обеих сторон и верхних, и нижних холмиков. При этом у пациентов с ППРС по отношению к ВПРС не было выявлено зон большей атрофии.
Выраженная атрофия таламуса при РС может иметь несколько механизмов: во-первых, из-за воспалительных изменений в самом таламусе и прямого нейродегенеративного процесса, а во-вторых, в результате непрямого поражения СВ (таламус является так называемым барометром диффузного нейродегенеративного процесса при РС, так как благодаря хорошо развитым реципрокным связям с корой и подкорковым СВ таламус чувствителен к их повреждению) [26]. Также наличие более выраженной атрофии подкорковых структур по сравнению с корой головного мозга, особенно у пациентов с КИС, говорит о вероятной атрофии глубоких отделов СВ в результате повреждения аксонов, нежели прямого воздействия [27]. Это также подтверждается тем, что при поражении зрительной лучистости отмечается атрофия латерального коленчатого тела [28].
Паттерны атрофии головного мозга при различных типах течения РС
Атрофия спинного мозга
Клиническая картина РС чрезвычайно гетерогенна, а симптоматика, которая возникает в результате повреждения спинного мозга (СпМ), часто доминирует и на определенном этапе отмечается у 90% больных [34]. В СпМ выявляются как локальные, так и диффузные очаги демиелинизации. У пациентов с КИС и ДТРС количество очагов меньше, чем при РРС, ВПРС и ППРС, что, вероятно, обусловливает и более легкое течение заболевания. При этом в исследованиях показано [35, 36] отсутствие корреляции между количеством очагов, выявляющихся в режиме Т2-ВИ, и атрофией, что говорит об их небольшой роли в развитии атрофии СпМ.
Атрофические изменения наиболее часто выявляются в шейном отделе СпМ, причем в большей степени у пациентов с прогрессирующим типом течения РС. Существует связь между степенью атрофии СпМ и тяжестью клинической симптоматики [37, 38]. Учитывая небольшой размер СпМ и строение окружающих тканей, измерять его объем довольно сложно. Однако с применением МРТ-морфометрии это стало возможным. Выраженная атрофия СпМ отмечается у пациентов с ВПРС, ППРС и даже при ДТРС [34]. Это подтверждает то, что атрофия развивается при прогрессирующем и длительно текущем заболевании. При данных типах течения РС отмечается одинаковое уменьшение объема на всем протяжении шейного отдела СпМ, при этом на каждом отдельном уровне оно больше выражено в задних и латеральных отделах его поперечника. Это подтверждается также и с помощью других методов и режима Т1-ВИ с применением импульса переноса намагниченности. У пациентов с ДТРС отмечается меньшая степень атрофии в целом по сравнению с пациентами с ВПРС, что говорит о том, что чем меньше выражены дегенеративные процессы, тем доброкачественнее протекает РС. Это также подтверждается наличием корреляций между выраженностью атрофии СпМ при ППРС и ВПРС и степенью нетрудоспособности по функциональной шкале EDSS.
При ППРС наблюдается выраженная атрофия СпМ, особенно задних его отделов, по сравнению с пациентами с КИС, РРС и группой контроля, несмотря на небольшую длительность заболевания. Тем не менее атрофия СпМ при ППРС менее выражена, чем при ВПРС; хотя оба этих типа течения РС являются прогрессирующими, выявленные отличия подтверждают различные механизмы их развития.
Корреляции атрофических изменений и клинических симптомов
В настоящее время именно атрофия ЦНС (головного и спинного мозга) считается ответственной за неуклонное прогрессирование как очаговой неврологической симптоматики, так и когнитивных нарушений [8]. С помощью применения гистологических и нейровизуализационных методик доказана наибольшая корреляция ряда клинических симптомов с изменениями СВ по сравнению с БВ или головным мозгом в целом 40.
Корреляции атрофии головного мозга с развитием инвалидизации
Согласно ряду данных [42], существуют корреляции между баллом по шкале EDSS и общей толщиной коры головного мозга, коры левых пре- и постцентральных, правой парагиппокампальной и левой латеральной затылочной извилин, а также с объемом правого хвостатого ядра и правого прилежащего ядра (группа нейронов в вентральной части полосатого тела). В некоторых работах показано, что у пациентов со стойким прогрессированием нетрудоспособности по шкале EDSS отмечается значительно более высокая скорость атрофических процессов по сравнению с пациентами со стабильной неврологической симптоматикой. Также считается, что объем СВ по сравнению с объемом БВ является более чувствительным предиктором инвалидизации, оцениваемой по шкале EDSS [43]. Противоположные данные были получены в исследовании A. Ceccarelli [44], в котором у пациентов с РС не было выявлено связи между локальным поражением СВ и оценкой по шкале EDSS. У пациентов с ДТРС также не отмечено связи между атрофией СВ, продолжительностью заболевания и оценкой по EDSS [45]. Корреляций между изменением объема БВ и клинической симптоматикой также выявлено не было.
Корреляции атрофии головного мозга с когнитивными нарушениями
Когнитивные нарушения, включающие снижение памяти, внимания и скорости воспроизведения информации, отмечаются у 70% пациентов с РС, причем они возникают уже на ранних стадиях заболевания (в течение первых 3 лет). У пациентов с РРС с когнитивными нарушениями по сравнению с пациентами без таковых выявляется снижение объема головного мозга в целом, а также СВ коры головного мозга. Действительно, корковая атрофия является предиктором когнитивных нарушений, потому что даже легкие когнитивные изменения связаны со значительным истончением коры головного мозга [47]. Также значительная корреляция была обнаружена и с атрофией таламуса.
Существуют данные о том, что атрофия головного мозга в меньшей степени влияет на когнитивные нарушения у пациентов с высоким «когнитивным резервом», который является результатом высокого уровня образования и интеллекта.
Корреляции атрофии головного мозга с утомляемостью
У пациентов с РС частым симптомом (до 80% случаев) является утомляемость. Она не связана с прогрессированием заболевания, степенью нетрудоспособности или локализацией очагов, но, вероятно, имеет связь с лобно-таламо-базальной сетью [48]. Исследования на данную тему немногочисленны. При сравнении пациентов с утомляемостью и без нее у первых была обнаружена атрофия вещества супратенториальных отделов головного мозга, включая кору, прилежащее БВ и головки хвостатых ядер, т.е. областей, которые функционально связаны с контролем внимания [49]. Авторы предполагают, что нарушение центральной моторной активации может быть связано с повреждением корково-подкорковых путей, включающих моторную кору. Так, 222 пациента с РРС с низкими баллами по шкале EDSS (не более 2) были разделены на две группы: пациенты с высокой степенью утомляемости (FSS не менее 5) и пациенты с низкой степенью утомляемости (FSS не более 4). В 1-й группе отмечались меньший объем СВ и БВ и наибольшее количество очагов в режимах Т2-ВИ и Т1-ВИ. Авторы предположили, что атрофия СВ и БВ может быть фактором риска появления утомляемости, которая при этом не связана со степенью нетрудоспособности.