Пункция головного мозга у ребенка
Забор нужного объема спинномозговой жидкости чаще всего используется для снижения внутричерепного давления ребёнка или для введения ему лекарственных препаратов. Пункция производится специальной стерильной одноразовой иглой. После проведения манипуляции ребёнок должен находиться в горизонтальном положении в течение 2-х часов. Как правило, манипуляция переносится детьми хорошо.
Люмбальную пункцию с уверенностью можно назвать одним из самых информативных способов диагностики патологии центральной нервной системы. В последние пару десятков лет число проведенных люмбальных пункций несколько уменьшилось из-за широкого распространения неинвазивных диагностических методов — компьютерной и магнитно-резонансной томографии. При этом, ряд заболеваний требуют качественного и количественного анализа спинно-мозговой жидкости – ликвора.
При проведении спинномозговой пункции ребёнка укладывают на бок спиной к врачу или усаживают с максимально согнутой спиной. Для наибольшей неподвижности обследуемого, его помогает удерживать ассистент. Чаще всего манипуляция проходит под общим наркозом.
В целом, люмбальную пункцию можно считать безопасным способом диагностики и лечения. Родителям и детям не стоит бояться этой манипуляции, ведь ее результат может ответить на многие сложные вопросы о характере патологии, вариантах лечения, а также прогнозе на будущее.
Гидроцефалия
Суть гидроцефалии в увеличении объема спинномозговой жидкости, и, как правило, повышении внутричерепного давления, вследствие нарушения баланса между выработкой и всасыванием цереброспинальной жидкости.
Гидроцефалия может быть как врожденной таки и приобретенной. Приобретенная гидроцефалия возникает вследствие опухолевой обструкции ликворпроводящих путей, травмы, внутричерепного кровоизлияния или инфекционного поражения оболочек головного мозга.
Патофизиология – гидроцефалия развивается по следующим причинам:
В разных возрастных группах гидроцефалия клинически проявляется по разному.
Острая гидроцефалия клинически проявляется выраженной головной болью, нарушением походки, тошнотой, зрительными нарушениями. У детей ранними признаками гидроцефалии могут быть раздражительность и неспособность удержать голову. При расширении третьего желудочка у больного проявляется синдром Парино (парез взора вверх – неспособность поднять глаза вверх) или симптом заходящего солнца (синдром Парино с ретракцией век и насильственным поворотом взора книзу). Редко может быть очаговый симптом в виде пареза отводящего нерва. У детей выбухает родничок, расширяются вены скальпа, прогрессивно увеличивается окружность головы. При прогрессировании патологии возникают симптомы поражения ствола головного мозга, кома, гемодинамические нарушения.
При нормотензивной гидроцефалии (гидроцефалия с нормальным внутричерепным давлением) симптоматика достаточно четкая. Она развивается, как правило у больных в преклонном возрасте.
Показания
При симптоматической гидроцефалии необходимо лечить основное заболевание.
Противопоказания
Не всегда гидроцефалию нужно лечить.
Исследования
Диагностические процедуры
Люмбальная пункция применяется для измерения внутричерепного давления. Но она должна быть выполнена после МРТ или КТ головного мозга.
Лекарственное лечение
Оказывает временный эффект. В транзиторных случаях, как окклюзия синуса, менингит, неонатальное вентрикулярное кровоизлияние, лекарственное лечение может быть эффективным. Применяются следующие препараты.
Предоперационные детали
Хирургическое лечение
Послеоперационное ведение больных
Осложнения
Результаты
Результаты зависят от многих факторов – характера основной патологии, продолжительности гидроцефалии, исходного состояния больного.
При своевременной и правильно выполненной операции результаты как правило в основном хорошие.
Острые нейроинфекции и их последствия
Острые нейроинфекции и их последствия. Инфекционные поражения нервной системы – одна из часто встречающихся форм неврологической патологии, которая составляет не менее 42% всех заболеваний этой сферы.
Нейроинфекция головного мозга классифицируется в зависимости от локализации патологического процесса, исходя из чего, различают:
энцефалит (воспаление ткани головного мозга, обусловленное инфекцией); миелит (воспалительный процесс спинного мозга, вызванный болезнетворными микроорганизмами); арахноидит (инфекционное воспаление затрагивает паутинную мозговую оболочку); менингит (инфекционное воспаление распространяется на оболочки мозга).
Кроме перечисленных видов нейроинфекции, развиваются и комбинированные патологии, например, энцефаломиелит, менингоэнцефалит.
Сочетанные формы инфекции нервной системы диагностировать намного сложней, несмотря даже на то, что в последние годы возможности диагностики нейроинфекций значительно улучшились.
В зависимости от длительности патогенного процесса, различают острое (менингит, энцефалит), подострое и хроническое (арахноидиты, арахноэнцефалиты) течение инфекционного поражения центральной нервной системы.
Основной путь передачи – воздушно — капельный: инфицирование чаще всего происходит при контакте с вирусоносителем, больным человеком, во время его кашля или чихания. Передается инфекция, в том числе, посредством поцелуя, если слюна попала на слизистую оболочку здоровых людей.
Предрасполагающим фактором является наличие эрозий на деснах или их воспаление, а также микроскопические травмы слизистого эпителия полости рта – при актуальности перечисленных обстоятельств, болезнетворному возбудителю будет проще проникнуть в организм и начать циркулировать в нем, развивая инфекцию.
Гематогенный путь инфицирования – не менее распространенный. Патологический процесс переходит на головной и спинной мозг в том случае, когда в организме имеется очаг хронической инфекции, в том числе, поражение сосудов, снабжающих эти важные центры. Такими предрасполагающими патологиями являются отит, абсцесс мозга, тромбоз синусов мозга.
Нейроинфекция развивается, в том числе из-за лимфогенного пути передачи, когда в организме пациента присутствуют скрытые осложнения перенесенных черепно-мозговых и спинномозговых травм. Особенно, если это отягощено ликвореей.
Инфекция не передается контактно-бытовым путем, поэтому, если использовать личные средства и вещи вирусоносителя, заражение не произойдет. Сезонность патологии – жаркое лето – такое условие является наиболее благоприятным для распространения инфекции, поэтому поражению нейроинфекцией больше подвержены населенные места с засушливым, знойным климатом.
Обобщая, следует отметить, что инфекция, поражающая нервную систему, может быть вызвана как вирусной, бактериальной, так и грибковой этиологией.
Озвучивая диагноз, учитывая происхождение возбудителя, проникновение которого в организм дало начало инфекции. Поэтому конкретизируют «бактериальный», «вирусный», «грибковый» (менингит, энцефалит и т. д.)
Причинами нейроинфекции головного мозга являются:
Перенесенные черепно-мозговые травмы (особенно, сопровождающиеся длительной компрессией); переохлаждение (пребывание на воздухе низкой температуры без головного убора); если во время проведения оперативных вмешательств на головном или спинном мозге, использовались медицинские инструменты или расходный материал, некачественного уровня стерилизации; если хирургическое или терапевтическое вмешательство осложнилось нарушением целостности перчаток врача или осуществлялось без их применения; перенесенные вирусные заболевания (чаще – грипп).
Нейроинфекция нередко возникает как внутрибольничное заболевание и может стать следствием посещения стоматолога, который во время работы использовал недостаточно продезинфицированные инструменты.К предрасполагающим факторам относится:
низкий иммунитет (особенно, если у пациента ВИЧ, туберкулез, сифилис или другие заболевания, подрывающие защитные свойства организма); наличие очагов гнойной инфекции (тонзиллит, отит), их скрытое течение или стремительный переход из острой стадии в хроническую форму; игнорирование контрольного обследования после перенесенных заболеваний, а также черепно — или спинномозговых травм.
В неврологической практике встречаются следующие виды инфекции нервной системы.
Менингит — воспаление оболочек головного и/или спинного мозга. Инфицирование происходит гематогенным, лимфогенным или воздушно-капельным путем.
Болезнетворные возбудители – вирусы, бактерии, грибы; предрасполагающими факторами являются наличие (в том числе скрытых) гнойных или воспалительных хронических процессов в пазухах носоглотки или слуховом канале, а также переохлаждение организма.
Симптомы менингита – достаточно специфические: визуализируя их, можно максимально быстро диагностировать этот вид нейроинфекции, приступив к ее лечению.
Наиболее выраженные проявления:
ригидность мышц затылка (пациент не может наклонить голову вперед); интенсивная головная боль, которая всегда сопровождается рвотой (этот симптом вызывает сомнение специалистов относительно того, менингит ли у пациента или же сотрясение мозга – определяющим фактором является анамнез); повышение температуры тела до высокой отметки.
Лечение предполагает постельный режим и антибиотикотерапию лекарственными препаратами антимикробного широкого спектра действия. Прогноз – благоприятный.
Арахноидит — воспалительный процесс, локализация которого – в паутинной оболочке головного мозга. Развитие арахноидита обусловливают перенесенные травмы головы, наличие ревматизма, своевременно не вылеченной ЛОР-инфекции.
Симптомами этого вида нейроинфекции являются:
сильная, устойчивая головная боль, лишающая возможности выполнять даже элементарные действия; ухудшение зрения; слабость; тошнота, приступ которой завершается рвотой; повышение температуры тела; возможно развитие носового кровотечения из-за нарушения мозгового кровообращения; бессонница; в тяжелых случаях – нарушение сознания или его отсутствие.
Прогноз для пациента благоприятный лишь в том случае, когда своевременно установлен диагноз и выполняется лечение. Терапия этой болезни направлена на устранение воспалительного процесса, стабилизацию мозгового кровообращения и общее укрепление организма пациента.
Энцефалит — воспаление ткани головного мозга является следствием клещевого поражения, а также проникновения и воздействия бактерий и вирусов. Если пациент пренебрегает обращением за медицинской помощью – прогноз неблагоприятный и даже летальный. Симптомы этого вида нейроинфекции ярко выражены:
головная боль усиливается в положении лежа, устойчива (плохо и кратковременно купируется анальгетиками); происходит повышение температуры тела; нарастает слабость и чувство разбитости, как проявления общей интоксикации организма.
лазодвигательные расстройства – часть симптомокомплекса, характерного для этого вида нейроинфекции: у пациента формируется птоз (опущение века), ощущение двоения в глазах, общее нарушение зрения.
Диспепсия проявляется тошнотой, которая особенно часто возникает после передвижения транспортом; возникает рвота.
Госпитализация предполагает дальнейшую терапию антибиотиками, гормональными препаратами и общеукрепляющими средствами.
Наиболее информативным видом исследования является МРТ, КТ, а также энцефалограмма. Лабораторная часть диагностики предполагает исследование крови и мочи.
Также проводится анализ спинномозговой жидкости – ликвора, в котором определяется повышенный уровень белка. Каждая из этих диагностических процедур позволяет визуализировать состояние головного и спинного мозга, определить локализацию патогенного процесса, степень инфицирования и вовлечения в воспалительный процесс тканей.
Лечение нейроинфекции сводится к следующему:
Установив диагноз, больного госпитализируют. Выполняется катетеризация вены (устанавливается постоянный внутривенный катетер). Назначается антибиотикотерапия. Антимикробный препарат выбирается врачом с учетом того, какой возбудитель спровоцировал развитие нейроинфекции: только придерживаясь этого, можно рассчитывать на успешность лечения. Антибиотики вводят внутривенно или капельно (посредством инфузий), поскольку это обеспечивает мгновенно попадание лекарственного вещества в кровь, в отличие от выполнения внутримышечных инъекций. Среди часто используемых препаратов – Цефепим, Медаксон, Цефтазидим. Пациенту назначают гормональные препараты – в основном, Преднизолон и Дексаметазон, дозировку которых определяется степенью тяжести пациента и формой патологии. Если нейроинфекция сочетанная, то дозировка гормонального вещества должна быть выше, чем при отдельном инфекционном заболевании нервной системы. Иммунитет пациента поддерживают введением витаминных комплексов. Коррекция уровня артериального давления проводится посредством введения сернокислой магнезии. Для того чтобы снизить степень отека мозга, больному вводят мочегонные средства: Фуросемид, Лазикс. На протяжении всего пребывания пациента в больнице, проводится мониторинг жизненных показателей его организма. Поддержание их на нормальном уровне обеспечивает постоянная инфузионная терапия пациента солевыми растворами и глюкозой. Проводят контроль диуреза больного. В целях профилактики истощения, выполняется парентеральное питание больного; осуществляют гигиенический уход. К наиболее тяжелым последствиям нейроинфекции относится летальный исход; инвалидность; слабоумие. Эти последствия являются веским основанием не откладывать обращение за медицинской помощью, пройти обследование и выполнять все назначения врача.Предупредить развитие нейроинфекции возможно: для этого следует своевременно лечить ЛОР и стоматологические патологии, избегать контакта с инфицированными людьми, надевать голвной убор при низкой температуре воздуха и укреплять иммунитет.Нейроинфекции — что это такое? Каковы причины развития таких заболеваний, эффективные пути лечения? С такими вопросами сталкиваются люди, которые впервые услышали от врача, что у них развивается нейроинфекция.В медицинских справочниках это заболевание трактуется как инфекционное, вызванное грибками, вирусами или бактериями, которое поражает нервную систему, при этом имеет тяжелое течение с высоким процентом смертности.Нейроинфекция включает в себя достаточно большой список заболеваний, многие из которых губительны для головного мозга. Все они могут иметь острую форму течения или переходить в хроническую и протекать достаточно вяло. Как показывает медицинская практика, эти заболевания могут пройти в острой форме один раз и больше не беспокоить больного или иметь частые и яркие рецидивы до конца его дней.Среди всех заболеваний этой группы к острым формам относятся:
Энцефалит — воспаляется вещество головного мозга. Самой частой причиной становится вирус клещевого энцефалита. Менингит — воспаляется оболочка мозга. Здесь может поражаться как головной, так и спинной мозг. Столбняк. Бешенство. Миелит — воспаляется спинной мозг из-за запущенной в нем инфекции. Арахноидит — воспаляется арахноидальная оболочка головного мозга.
К хроническим формам относят:
нейросифилис; нейроСПИД; проказа; поражение нервной системы туберкулезом; нейробруцеллез; бруцеллез.
Независимо от вида и места поражения, нейроинфекция головного и спинного мозга проявляется тремя яркими симптомами:
Общая интоксикация организма. У больного резко поднимается температура тела, очень часто до критических отметок, появляется общая слабость в организме, снижается трудоспособность. Ликворный синдром. В клетках ликворы значительно увеличивается количество белка и клеток, которые превалируют над белками. Симптомы ликворной гипертензии. Больные указывают, что в положении лежа у них значительно усиливается головная боль, особенно в утренние часы, может отмечаться спутанность или рассеянность сознания, бывают случаи тахикардии и пониженного артериального давления.
Миелит. Этот вид нейроинфекций считается одним из самых тяжелых и опасных для человека. При поражении спинного мозга практически всегда остаются серьезные осложнения: гибнут нервные клетки, что приводит к параличу, нарушениям функций кишечника, мочевого пузыря.В качестве лечения будут использоваться препараты группы глюкокортикостероидов и антибиотики широкого спектра действия. Очень важно проходить своевременное лечение в стационаре, чтобы сразу останавливать развитие сопутствующих заболеваний, которые будут активироваться на фоне миелита.Так как практически во всех случаях при миелите наступает паралич, то крайне важно организовать правильный уход за больным и его кожей, использовать средства, которые предотвращают появление пролежней.
У взрослого человека после перенесенных заболеваний остается головная боль, постоянные болевые ощущения в спине, которые усиливаются при изменении погоды. Многие медики также констатируют, что у таких больных после выздоровления ухудшается память, отмечаются проблемы с запоминанием, может нарушаться слух, зрение. Встречаются единичные случаи, когда нейроинфекционное заболевание приводит к полной инвалидизации, человек теряет зрение или слух.
Однако для уточнения диагноза и определения места поражения используют лабораторные и инструментальные методы:
Методы нейровизуализации: компьютерная и магнитно-резонансная томография, позволяют оценить состояние ткани ЦНС, мозговых оболочек. Электроэнцефалография используется для оценки функционирования клеток головного мозга и позволяет выявить распространенность и тяжесть поражения нервной ткани. Электронейромиография применяется для выявления степени тяжести поражения проводящих нервных путей при наличии у пациента парезов или параличей. Люмбальная пункция с последующим анализом спинномозговой жидкости позволяет выявить воспалительный процесс в ЦНС, определить его возбудителей (вирусы или бактерии). Клинический и биохимический анализ крови способствуют выявлению воспалительного процесса в организме. Правильное использование описанных методов совместно со сбором жалоб и проведением неврологического осмотра позволяет ставить верный диагноз и назначить рациональное лечение.
«Бомбу замедленного действия» представляют собой аневризмы сосудов головного мозга, а именно выпячивание истонченного участка стенки кровеносного сосуда. Разрыв аневризмы представляет угрозу для жизни в виде геморрагического инсульта или субарахноидального кровоизлияния. Проявляется резкой, внезапно начавшейся, головной болью (кинжальной), так проявляется спазм сосудов реагирующих на излившуюся кровь
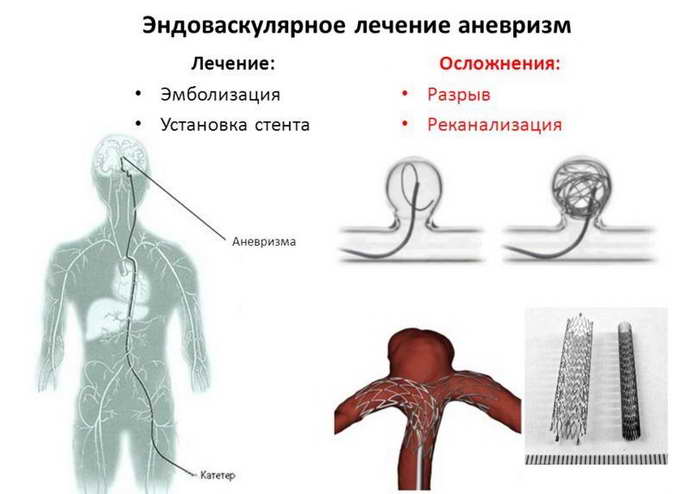
Хирургическая операция является единственным эффективным методом лечения аневризмы сосудов головного мозга. Получив результаты обследований пациента, врач принимает решение о тактике проведения операции. Так как, последствия разрыва аневризмы сосудов головного мозга часто носят летальный характер, проведение оперативного вмешательства может сохранить жизнь пациенту. Оперативное лечение возможно провести как «открытым», так и малоинвазивным способом в зависимости от показаний. «Открытые» операции требуют трепанации черепа, долгой микрохирургической операции и клипирования аневризмы – исключения ее из кровотока.
«Современные технологии эндоваскулярной нейрохирургии дают возможность делать эти операции без трепанации черепа. Через бедренную артерию по всему организму мы проводим специальные катетеры, заходим в аневризму и устанавливаем в нее специальные спирали, после чего аневризма «выключается» (атрофируется) из кровотока и таким образом исчезает риск кровоизлияния», – поясняет заведующая отделением рентгенхирургических методов диагностики и лечения Татьяна Леонидовна Дашибалова.
Бескровные операции – не новинка для бурятских нейрохирургов и рентгенхирургов, в Республиканской клинической больнице им. Н.А.Семашко их выполняют около 8 лет. Однако существуют аневризмы, которые невозможно оперировать открытым методом, в этом случае приходит на помощь метод эндоваскулярной окклюзии (эмболизации). Для передачи бесценного практического опыта в РКБ на один день из Новосибирска приехал один самых известных нейрохирургов России, к.м.н., Виталий Сергеевич Киселев, работающий в ФГБУ «Федеральный центр нейрохирургии». Врачи-рентгенхирурги Арюна Цыденова и Зоригто Балханов с участием Виталия Киселева успешно выполнили эндоваскулярные операции у 5 пациентов со сложными аневризмами. Одному из пациентов был установлен специальный поток перенаправляющий стент с эмболизацией полости аневризмы.
С раннего утра и до позднего вечера в операционной кипела работа. Пристально вглядываясь в мониторы, команда врачей и медсестер устраняла опасные аневризмы. Все манипуляции проводятся под рентген-телевизионным контролем под большим увеличением. Сначала хирург делает прокол в области передней поверхности бедра вблизи паховой связки для доступа к бедренной артерии, в артерию устанавливается интродьюсер – небольшая эластичная трубочка с клапаном, через которую затем проводятся все остальные инструменты, не травмируя стенку артерии. После этого вводится специальный катетер – более длинная и узкая трубочка со специфической конфигурацией её кончика – проводится при помощи проводника в интересующие артерии, через катетер доставляют контрастное вещество, которое хорошо визуализируется под рентгеновским излучением, проводится трехмерная ангиография с компьютерной реконструкцией изображения в объеме, находится аневризма. Далее в полость аневризмы также с помощью проводника вводят микрокатетер.
На втором шаге, как только кончик микрокатетера окажется в полости аневризмы, из микрокатетера высвобождается микроспираль, которая изменяет свою форму, и в виде беспорядочного мотка проволоки занимает собой полость аневризмы. При больших размерах аневризмы может понадобиться несколько спиралей. Заполненная проволочной спиралью аневризма выключается из кровотока и постепенно зарастает соединительной тканью, то есть, исключается возможность ее разрыва.
На заключительном этапе инструменты последовательно извлекаются из сосудистого русла, область пункции бедренной артерии ушивается специальным устройством. Сутки после вмешательства пациент наблюдается в реанимации.
Ежегодно в России примерно у 15 человек из каждых 100 тысяч происходит разрыв аневризмы (выпячивания стенки сосудов мозга), и около 15% таких больных погибает, не успевая доехать до больницы. У половины пациентов кровоизлияние повторяется в течение последующих шести месяцев — в этом случае смертность достигает 70%. И хотя частота таких аномалий высока — их можно диагностировать с помощью МРТ в сосудистом режиме, КТ с контрастированием, а благодаря современным технологиям пациент возвращается домой уже через пару дней после операции.
Пункция головного мозга у ребенка
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция; Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова; Университет медицины и фармации им. Николая Тестемицану Республики Молдова, Кишинев, Республика Молдова
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Университет медицины и фармации им. Николая Тестемицану Республики Молдова, Кишинев, Республика Молдова
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2018;118(11): 87-92
Конческу Д., Молдовану И., Одобеску С., Мавет Дж., Русева А., Вовк В., Рооз К. Постпункционный синдром. Журнал неврологии и психиатрии им. С.С. Корсакова. 2018;118(11):87-92.
Concescu D, Moldovanu I, Odobescu S, Mawet J, Ruseva A, Vovc V, Roos C. Post-lumbar puncture syndrome. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2018;118(11):87-92.
https://doi.org/10.17116/jnevro201811811187
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция; Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
В статье представлен клинический случай, в котором авторы описывают определенные клинические аспекты, факторы риска, лечение и методы профилактики осложнений постпункционного синдрома.
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция; Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова; Университет медицины и фармации им. Николая Тестемицану Республики Молдова, Кишинев, Республика Молдова
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция
Институт неврологии и нейрохирургии, Кишинев, Республика Молдова
Университет медицины и фармации им. Николая Тестемицану Республики Молдова, Кишинев, Республика Молдова
Центр головной боли, госпиталь Ларибуазьер, AP-HP, Париж, Франция
Поясничная пункция является диагностической, а иногда и терапевтической процедурой, выполняемой с целью забора ЦСЖ для биохимического, микробиологического и цитологического анализов или, что реже, для уменьшения внутричерепного давления. Процедура часто выполняется при острых состояниях, для того чтобы исключить наличие опасных заболеваний, таких как менингит, энцефалит, субарахноидальное кровоизлияние, или в терапевтических целях в случае псевдотуморозного синдрома или при синдроме повышения внутричерепного давления.
Еще во II веке н.э. греческий врач Гален выдвинул гипотезу o существовании желудочков головного мозга, содержащих газ, — так называемую душевную пневму. Только в XIX веке F. Magendie (Мажанди) [1] наглядно продемонстрировал существование ЦСЖ, пропунктировав большую цистерну головного мозга у животных, тем самым доказав существование субарахноидального пространства, которое соединяется с IV желудочком. В 1891 г. Квинке [цит. по 2] выполнил первую поясничную пункцию у человека, а в 1898 г. A. Bier [3] впервые описал постпункционный синдром (ППС).
ППС может осложнить все типы пункции твердой мозговой оболочки (поясничная пункция, рахианестезия или эпидуральная анестезия). Он чаще встречается у молодых лиц [4], женщин [5, 6] с низкой или нормальной массой тела [7], у пациентов, имевших ранее в анамнезе первичные головные боли (мигрень, головная боль напряжения) [5, 8], а также тревожные состояния [9]. Частота диагностической поясничной пункции составляет 15—40%, рахианестезии — 7,5%, и эта процедура чаще используется в акушерской практике или по другим показаниям [7]. Частота случайной пункции твердой мозговой оболочки при эпидуральной анестезии составляет от 0—2,6%, тогда как частота ППС доходит до 70% [10, 11].
Клинический случай. Пациентка 33 лет поступила в Центр головной боли (Париж) 28.01.14 с головной болью, возникшей с 30.12.13. Женщина происхождением из Шри-Ланки, мать 3 детей, последние роды 30.12.13 естественным путем с эпидуральной анестезией. Сразу после родов пациентка стала предъявлять жалобы на сильную сдавливающего характера головную боль, локализованную в лобной области, с иррадиацией в затылочную и шейную области. В начале отмечала уменьшение головной боли в положении лежа. Предложенные гинекологом методы лечения обезболивающими средствами (аспирин, нестероидные противовоспалительные средства) и триптанами давали незначительный эффект, больная была выписана домой под наблюдение семейного врача.
В дальнейшем головная боль стала постоянной, потеряв ортостатический компонент, что привело к бессоннице с частыми пробуждениями из-за боли. По этой причине больная обратилась в Центр головной боли парижской клиники Ларибуазьер (практически через 1 мес от дебюта головной боли). Интенсивность головной боли по визуальной аналоговой шкале боли достигала 8/10 баллов. Боли были диффузными, иррадиирующими в шейный отдел. Температура тела и артериальное давление пациентки были нормальными, общий и данные неврологического осмотра — в пределах нормы, без менингеальных знаков. Пациентка не предъявляла жалоб на шум в ушах, гипоакузию или «заложенность в ушах».
Были выполнены КТ головного мозга без и с контрастированием (рис. 1), 
При МРТ головного мозга после болюсного введения гадолиниевого контрастного вещества (рис. 2) 
С учетом клинической картины постпункционной внутричерепной гипотензии вследствие эпидуральной анестезии, осложненной двусторонними субдуральными гематомами, пациентка была госпитализирована в отделение неврологии. Больная сохраняла горизонтальное положение в течение 48 ч, ей было предложено лечение кофеином, которое оказалось неэффективным.
Через 2 дня, 30.01.14, больной было проведено пломбирование эпидурального пространства аутокровью (ПЭПА) объемом 30 мл на уровне LII—LIII. Введение было приостановлено при появлении головной боли и боли в спине, что указывает на достаточный объем введенной крови в перидуральное пространство. В дальнейшем пациентка оставалась в положении лежа на спине в течение 3 ч. При переходе в вертикальное положение больная не предъявляла жалоб на головную боль, была выписана с рекомендациями продолжить лечение на дому, в частности прием комбинации парацетамола с кофеином 2—3 г/сут.
Еще через 1 мес, 03.02.14, больная снова вернулась в Центр головной боли из-за рецидива диффузных головных болей, иррадиирующих в затылок, шума в ушах, фонофобии, уменьшающихся в положении лежа, а также из-за появления болей в спине. Неврологический статус был без особенностей. На компьютерных томограммах головного мозга и ангиограммах, выполненных 03.02.14, отмечалась частичная резорбция субдуральных скоплений, без тромбоза мозговых вен. МРТ спинного мозга больной — без особенностей.
Принимая во внимание, что больная является матерью 3 малолетних детей и ей, видимо, было достаточно сложно соблюдать в полной мере рекомендации по профилактике ППС, мы предположили, что произошло новое истечение ЦСЖ. Ввиду этого было принято решение выполнить вторую процедуру пломбирования эпидурального пространства аутокровью объемом 15 мл на уровне LII—LIII. После процедуры состояние больной улучшилось. С учетом того, что у больной наблюдались сопутствующие проявления тревожно-депрессивного синдрома, в течение 3 дней были проведены капельницы с амитриптилином в дозировке 75 мг/сут. Течение заболевания было благоприятным, с исчезновением головной боли и других сопутствующих симптомов. Таким образом, больной был выставлен следующий клинический диагноз: 7.2.1. Головная боль в рамках постпункционного синдрома, осложненного двусторонними субдуральными гематомами.
Позднее, 06.05.14, через 3 мес, на контрольном осмотре больная не предъявляла жалоб на головные боли, а по данным контрольной МРТ головного мозга после болюсного введения гадолиниевого контрастного вещества (рис. 3) 
Патофизиология ППС. Циркуляция ЦСЖ осуществляется от хориоидального сплетения боковых желудочков по направлению к субарахноидальному пространству через цистерны основания и конвекситальные борозды, резорбируется в венозную систему на уровне грануляций паутинной оболочки (пахионовы грануляции) через механизм клапанной системы. Очень небольшое количество ЦСЖ резорбируется в сосудах головного мозга с помощью механизма диффузии.
Отверстие в твердой мозговой оболочке, образованное иглой, в случае медленного рубцевания ведет к вытеканию ЦСЖ в эпидуральное пространство [12]. Эта утечка может спровоцировать дисбаланс между количеством продуцируемой и утерянной ЦСЖ, индуцируя внутричерепную гипотензию [13].
Внутричерепная гипотензия проявляется ортостатической головной болью, которая уменьшается в положении лежа. Боль вызвана опущением структур головного мозга, сопровождаемым ассоциированным натяжением структур, чувствительных к боли (оболочки головного мозга, венозные сплетения и артерии основания черепа) и расширением венозных сплетений для компенсации утраченного объема ЦСЖ. Согласно теории Монро—Келли [14] объемы полости черепа и головного мозга не изменяются и гиповолемия ЦСЖ компенсируется увеличением обьема сосудистого компонента [15]. Отек ствола мозга (вазогенный отек) связан с уменьшением венозного оттока из-за «стеноза» синуса (ампулы Галена, или правого синуса). Кохлеовестибулярные симптомы (шум в ушах, гипоакузия, головокружение) можно объяснить изменением давления эндолимфы, зависимой от объема, давления ЦСЖ [16]. Вовлечение черепных нервов, включая VI, обусловлено смещением головного мозга вниз [10].
Клиническая картина. Основным проявлением ППС служит необычная головная боль, которая устанавливается в первые 5 дней после пункции твердой мозговой оболочки [10, 17, 18]. Характер дебюта головной боли прогрессирующий или острый, иногда взрывного типа, как при громоподобной головной боли, что, однако, встречается реже. Локализация вариабельная, чаще затылочная, лобная, височная или орбитальная, может изменяться в процессе развития головной боли (у >50% больных) [6, 10]. Пациенты могут оставаться в вертикальном положении не более нескольких минут, а движения головы или проба Вальсальвы, кашель, дефекация, зевание, вероятнее всего, будут усиливать головную боль [19]. В 70—85% случаев головная боль ассоциирована с другими признаками или симптомами, непроизвольно усиливающимися в вертикальном положении пациента и уменьшающимися в положении лежа [10] (табл. 1). 
Изменение характера первичных головных болей, особенно потеря ортостатического компонента с развитием нарушений сознания, очагового дефицита или судорог, может быть вызвано сдавлением промежуточного мозга, обусловленным птозом мозжечка, гематомой или церебральным венозным тромбозом. Частота развития тяжелых осложнений при ППС остается неопределенной [10].
Критерии диагностики головной боли при ППС согласно Международной классификации головных болей ICHD-3 (2013) [18]:
A. Все головные боли, соответствующие критерию C.
B. Проведение пункции твердой мозговой оболочки.
C. Возникновение головной боли в первые 5 дней после проведения пункции.
D. Головная боль не соответствует другим диагностическим критериям ICHD-3.
Радиологическая клиническая картина. В случае ортостатической головной боли важно провести МРТ головного мозга или/и спинного мозга с болюсным контрастированием гадолинием для выявления осложнений ППС, ассоциированного с прямыми признаками внутричерепной гипотензии: вытекание ЦСЖ через отверстие в твердой мозговой оболочке [20], контрастирование мозговых оболочек, краниокаудальное смещение головного мозга, дающее эффект псевдо-Киари, субдуральная гематома или гигрома, уменьшение объема желудочков и расширение венозных синусов. Существует очень мало публикаций, посвященных МРТ при ППС, поэтому длительность возникновения и исчезновения осложнений в соответствии с клиническими проявлениями до сих пор не известна. R. Gordon и соавт. [20] сообщают об исчезновении накопления контрастного вещества в течение 2 нед после лечения ППС. Сканирование головного мозга с болюсным контрастированием не подтверждает ППС, но может выявить субдуральные накопления: субдуральная гематома, гигрома или тромбоз вен головного мозга (табл. 2). 
Неблагоприятные факторы и профилактика ППС. Риск развития ППС преобладает у подростков и молодых людей; частота его развития в 3—4 раза выше у пациентов в возрасте 20—29 лет, чем в возрасте 50—59 лет [10]. Как исключение ППС встречается у пожилых людей ( 60 лет) [22], а также у детей [23].
Наличие в анамнезе эпизода ППС считается фактором риска (ФР) повторного его появления после поясничной пункции [22]. ППС в 2 раза чаще встречается у женщин, чем у мужчин, особенно при наличии тревожных расстройств [9], низкой массе тела (ожирение является защитным фактором) [5, 24] и прешествующих первичных головных болях [8].
Стало очевидно, что определенные механические параметры инструментария и процедуры проведения поясничной пункции остаются очень важными и их несоблюдение может привести к возникновению ППС: большой калибр иглы марки G20/22, «острая» форма кончика, извлечение иглы без введения мандрена, большой объем эвакуированной жидкости и др. (табл. 3). 
В 1902 г. были опубликованы первые методы профилактики ППС, которые заключались в вынужденном положении пациента лежа первые 24 ч после проведения пункции [24, 25]. Этот факт вынужденного положения был опровергнут результатами контрольного исследования 1981 г., продемонстрировавшего полную неэффективность такого подхода [26].
Лечение ППС. По данным разных авторов, без специфического лечения 72% больных с ППС восстанавливаются в течение 7 дней без какого-либо вмешательствa [7], а по данным другим авторов, 82% больных — в течение 6 мес [27].
Пломбирование эпидурального пространства аутокровью (ПЭПА) или «пломбирование дуральной бреши» в настоящее время является самым эффективным методом лечения в случае неудачного консервативного лечения ППС. Его эффективность по сравнению с консервативным лечением продемонстрирована в ходе многих рандомизированных исследований [28, 29]. Эффективность ПЭПА варьирует, согласно проведенным исследованиям, в пределах 77—96%, а в случае неудачного проведенного первого ПЭПА (