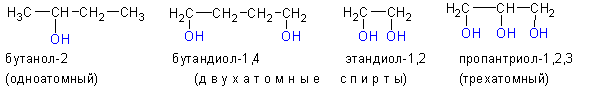
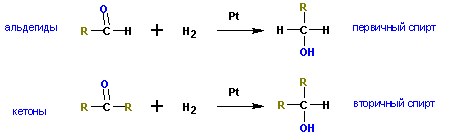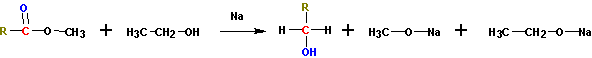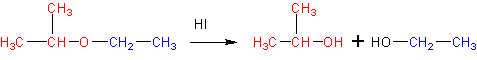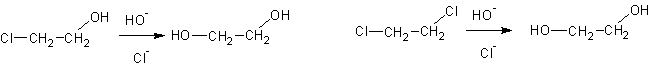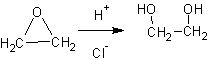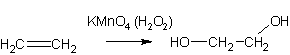Окисление вторичных спиртов
Вы будете перенаправлены на Автор24
Общим методом получения кетонов из вторичных спиртов является окисление их оксидом хрома (VI) в воде или разведенной уксусной кислоте. Хромовый ангидрид в ацетоне и дихроматы пиридиния можно использовать для окисления ненасыщенных вторичных спиртов, не нарушая двойных и тройных связей:
Вторичные спирты сложного строения, содержащие чувствительные к действию окислителей группы, можно с хорошими выходами окиснюваты в соответствующие кетонов, используя метод Оппенауера. В системе, содержащей вторичный спирт и кетоны (как правило ацетон) в присутствии алкоголятов алюминия устанавливается равновесие:
Готовые работы на аналогичную тему
Окисление ароматических спиртов
Окисление фенолов является сложным, многостадийным процессом, механизм которого мало изучен. Сам фенол окислением производными шестивалентного хрома, четырех и семи валентного марганца в серной кислоте образует с удовлетворительным выходом пара-хинон.
Вторичную гидроксильную группу ароматических спиртов можно окислять в карбонильную и при наличии в молекуле других заместителей, например, первичной спиртовой группы. Для этого, первичную гидроксильную группу защищают превращением в трифенилметиловий эфир (третичная защита) обработкой диола трифенил-хлорометаном в присутствии основания (пиридина) при комнатной температуре. Эфир, который образуеться, устойчивый в нейтральной и щелочной среде, а незащищенную вторичную спиртовую группу можно окислять диоксидом марганца. Третичную защиту снимают при нагревании с разбавленной уксусной или соляной кислотой:
Окислители для окисления вторичных спиртов
Расщепление α-гликолей
Механизм этой реакции полностью еще не выяснен. Как правило, цис-гликоли расщепляются значительно быстрее, чем транс- гликоли. Йодатная кислота, в отличие от тетраацетата свинца, растворима в воде и поэтому может быть использована в качестве реагента для расщепления нерастворимых в органических растворителях сахаров. Она используется для определения размеров колец гликозидов.
Спирты
Классификация спиртов
Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода), вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).
Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол, этанол, пропанол, бутанол, пентанол и т.д.
Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с простыми эфирами, которых мы также коснемся в данной статье.
Получение спиртов
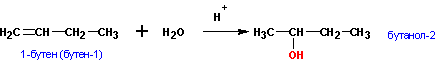
Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода, а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.
В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных химических соединений, в том числе и метанола.
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
Химические свойства спиртов
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.
Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.
В результате реакций спиртов с кислотами образуются различные эфиры.
Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при которых углеродный скелет подвергается деструкции.
Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой реакции выпадает маслянистый осадок.
Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор окрашивается в характерный синий цвет.
Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов). Это говорит об их более выраженных кислотных свойствах.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Во что окисляются вторичные спирты
Tомский государственный университет
кафедра органической химии
Кислородсодержащие соединения. Спирты
Строение и классификация спиртов
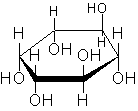
Среди многоатомных спиртов наиболее известен шестиатомный циклический спирт инозит :
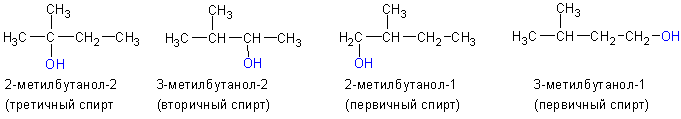
3. По положению гидроксильной группы в цепи различают первичные, вторичные и третичные спирты:
При наименовании спиртов по номенклатуре IUPAC находят самую длинную цепь атомов углерода, содержащую гидрокисльную группу, и нумеруют ее с края, к которому ближе гидроксильная группа. После перечисления заместителей добавляется название, соответствующее углеводороду главной цепи с добавлением окончания –о л и цифры, показывающей место гидроксильной группы в цепи (см. примеры выше).
Химические свойства спиртов
1. Реакции дегидратации спиртов (внутри- и межмолекулярная дегидратация)
При кипячении с кислотами спирты могут образовывать алкены и простые эфиры.
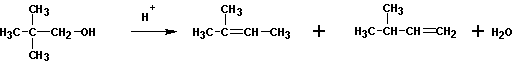

Как правило, получаются смеси продуктов. Преобладание того или иного соединения связано с условиями проведения реакции. Так, при повышении температуры выход алкенов увеличивается. Выходы алкенов также возрастают при переходе от первичных к третичным спиртам. Очень часто перечисленные реакции сопровождаются перестройками в углеродном скелете:
Образование простых эфиров (межмолекулярная дегидратация спиртов).
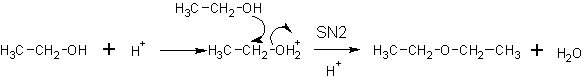
В присутствии серной кислоты:
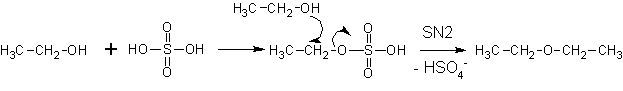
Пример получения метил-третбутилового эфира (МТБЭ) реакциями:
2. Образование галоидных алкилов из спиртов происходит при реакции с различными реагентами:
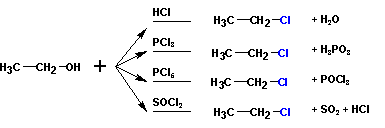
Во всех случаях наиболее гладко протекают реакции с первичными спиртами, третичные спирты чаще дают различные побочные продукты.
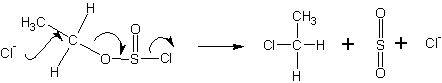
Механизмы галогенирования спиртов тионилхлоридом ( SOCl 2 ) и галогенидами фосфора
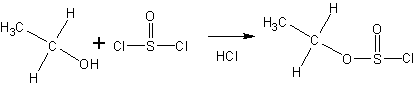
Тионилхлорид образует со спиртами эфиры хлорсернистой кислоты (хлорсульфиты ):
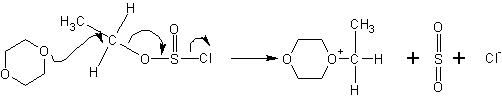
При этом генерируется некоторое (заметное) количество анионов хлора.
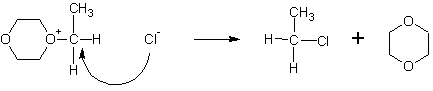
Полученное промежуточное соединение атакуется повторно анионами Cl- с противоположной стороны, в результате чего не происходит обращения оптической конфигурации (если сравнивать с исходным спиртом):
Однако, в таких растворителях, как пиридин или гексаметилфосфотриамид (НМРТ), концентрация свободных ионов хлора достаточно велика, чтобы атаковать эфиры хлорсульфита с образованием галогенпроизводных спирта с обращенной конфигурацией:
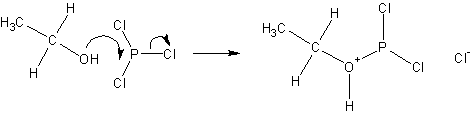
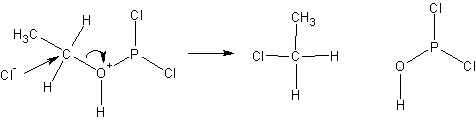
Реакции с галогенидами фосфора протекают с обращением конфигурации согласно ниже приведенной схеме;
После чего хлорид ио н- замещает группировку с атомом фосфора:
3. Кислотные свойства спиртов
При взаимодействии с сильными основаниями и щелочными металлами спирты ведут себя как кислоты:
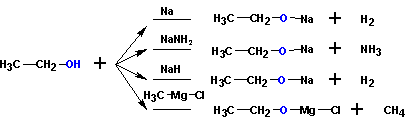
4. Окисление спиртов
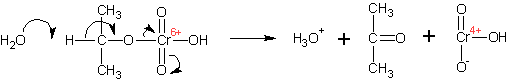
Спирты окисляются различными окислителями до альдегидов (первичные спирты) и кетонов (вторичные спирты). Механизм окисления спиртов хромовой кислотой:
Образующиеся вначале эфиры хромовой кислоты претерпевают отщепление протона от атома углерода, при котором стояла гидроксильная группа (вследствие повышения его кислотности в результате образования эфира, он отщепляется даже таким слабым основанием, как вода):
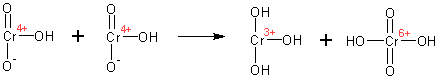
Образуется продукт окисления и хромистая кислота ( Cr IV ). Хромистая кислота быстро диспропорционирует до гидроокиси хрома ( Cr III ) и хромовой кислоты ( Cr VI ):
Если таким образом окисляются вторичные спирты, то образующиеся кетоны сравнительно устойчивы, однако, при окислении первичных спиртов образуются альдегиды, которые легко окисляются дальш е- до карбоновых кислот (если не предпринимать меры предосторожности). Альдегиды с небольшим числом атомов углерода можно выделить из реакционной смеси отгонкой в процессе получения, однако, для более тяжелых альдегидов такой способ не помогает.
Окисление спиртов реагентом Саретта ( Sarett )- смесью хромового ангидрида и пиридина позволяет выделять альдегиды.
5. Образование сложных эфиров
Сложные эфиры образуются при реакции спиртов с минеральными и органическими кислотами.
(Реакции протекают при умеренном нагревании, кислотный катализ).
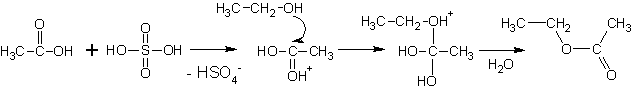
6. Образование ацеталей и полуацеталей
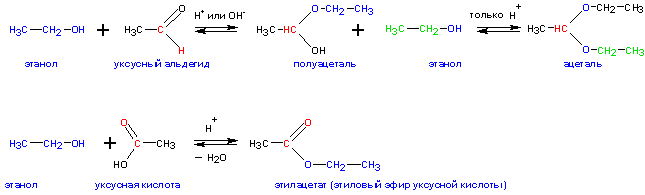
Спирты взаимодействуют с альдегидами и кетонами— с образованием полуацеталей и ацеталей (альдегиды) и полукеталей и кеталей (кетоны):
Ацетали представляют собой жидкости с приятным эфирным запахом.
Способы получения спиртов
1. Гидратация алкенов (правило Марковникова):
2. Гидролиз галоидных алкилов :
а) обратимый гидролиз в кислой среде;
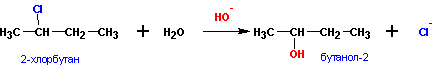
б) необратимый гидролиз в щелочной среде:
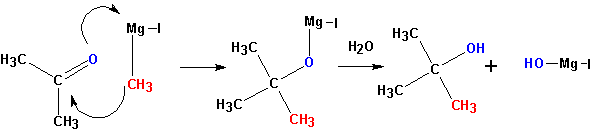
3. Взаимодействие металлорганических соединений (реактивы Гриньяра ) с карбонильными группами (нуклеофильное присоединение по кратной связи С =О):
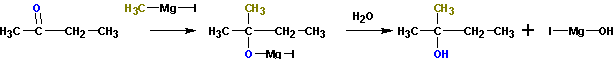
Из кетонов получаются третичные спирты. Так, из метилэтилкетона (бутанон-2) получается 2-метилбутанол-2. Альдегиды в подобной реакции дают вторичные спирты. Из пропионового альдегида (пропаналь ) получается бутанол-2:
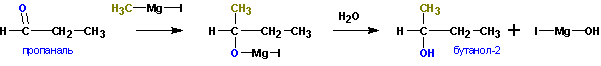
Из формальдегида образуются первичные спирты.
Взаимодействие реактивов Гриньяра со сложными эфирами карбоновых и муравьиной кислот ы- приводит к получению третичных и вторичных спиртов, соответственно.
Менее распространены способы получения спиртов восстановлением альдегидов и кетонов.
5. Восстановление сложных эфиров ( каталитические и некаталитические).
Получение спиртов восстановлением сложных эфиров по Буво-Блану (кипячение с натрием).
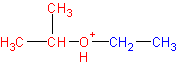
6. Расщепление простых эфиров HJ и HBr
Реакция представляет собой нуклеофильное замещение в алкил оксонии :
Реакции двухатомных спиртов (отличные от первичных спиртов реакции).
1. внутримолекулярная дегидратация :
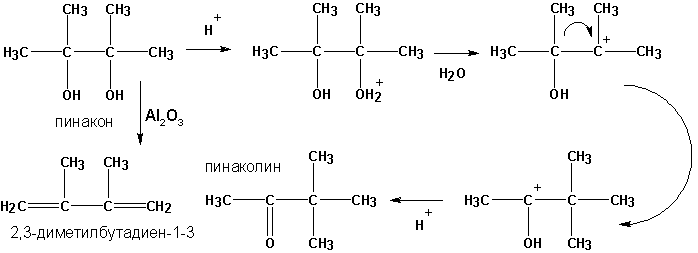
г) пинакон-пинаколиновая перегруппировка
д ) дегидратация пинаконов в присутствии окиси алюминия приводит к диенам:
а) образование спиртоэфиров
б) образование циклических эфиров:
Получение двухатомных спиртов
1. Гидролиз дигалогенпроизводных или хлоргидринов :
2. Гидратация альфа-окисей (эпоксидов ):
3. Окисление олефинов перекисью водорода или перманганатом (холодные растворы):
4. Каталитическое восстановление сложных эфиров дикарбоновых кислот:
Спирты и фенолы
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Классификация спиртов
По числу гидроксильных групп:
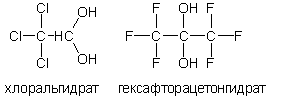
Двухатомные спирты с двумя и тремя гидроксогруппами у одного атома углерода R‒CH(OH)2 или R-C(OH)3 неустойчивы, от них легко отрывается вода и образуется карбонильное соединение.
Классификация по числу углеводородных радикалов у атома углерода при гидроксильной группе
Классификация по строению углеводородного радикала
Непредельные спирты, в которых гидроксильная группа соединена с атомом углерода при двойной связи (алкенолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения.
Строение спиртов и фенолов
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения метанола +64,5 о С). Температуры кипения многоатомных спиртов и фенолов значительно выше.
Таблица. Температуры кипения некоторых спиртов и фенола.
| Название вещества | Температура кипения |
| Метанол | 64 |
| Этанол | 78 |
| Пропанол-1 | 92 |
| Бутанол-1 | 118 |
| Этиленгликоль | 196 |
| Фенол | 181,8 |
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Низшие спирты (метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин) смешиваются с водой в любых соотношениях.
Номенклатура спиртов
Нумерация ведется от ближайшего к ОН-группе конца цепи.

Например: СН3ОН – метиловый спирт, С2Н5ОН – этиловый спирт и т.д.
Например, пропандиол-1,2 (пропиленгликоль):
Изомерия спиртов
Структурная изомерия
Для спиртов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета характерна для спиртов, которые содержат не менее четырех атомов углерода.
| Например. Ф ормуле С4Н9ОН соответствуют четыре структурных изомера, из них два различаются строением углеродного скелета |
| Бутанол-1 | 2-Метилпропанол-1 |
 |  |
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С2Н6О этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3 |
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
| Например. Пропанол-1 и пропанол-2 |
| Пропанол-1 | Пропанол-2 |
 |  |
Химические свойства спиртов
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н + соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
| Таким образом, для спиртов характерны следующие свойства: 1. Кислотные свойства
1.1. Взаимодействие с раствором щелочейПри взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой. Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей. Многоатомные спирты также не реагируют с растворами щелочей. 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)Спирты взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты. Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Многоатомные спирты также реагируют с активными металлами: 1.3. Взаимодействие с гидроксидом меди (II)Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
2. Реакции замещения группы ОН2.1. Взаимодействие с галогеноводородамиПри взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
|