Зачем колят гормоны при аллергии
Прежде чем говорить о том, что представляет собой гормонотерапия, и в каких случаях её назначают, хотим напомнить каждому, кто интересуется данной темой, вот о чём:
лечение гормональными препаратами может назначать только врач;
правильный подбор средства возможен лишь после полного обследования пациента;
у каждого гормонального препарата есть ряд противопоказаний;
курс терапии можно проходить исключительно под наблюдением специалиста.
Эти четыре пункта – первое, что нужно знать о гормональной терапии.
В организме среднестатистического человека железами внутренней секреции синтезируется около 50 гормонов. Точное их количество индивидуально и зависит от возраста, пола и состояния здоровья (человеческая эндокринная система способна производить до 74 видов гормонов). Данные вещества выделяются непосредственно в кровь и отвечают за такие процессы как рост, обновление тканей, обмен веществ, деторождение и прочие.
Нехватка либо избыток какого-либо гормона сигнализирует о неправильной работе (снижении или повышении активности) той или иной железы.
Существуют 4 группы гормонов:
нейросекреторные – синтезируются плацентой и нервными клетками гипофиза и гипоталамуса;
гландулярные – синтезируются щитовидной железой, надпочечниками и яичниками;
гландотропные – выделяются эндокринной системой;
тканевые, а именно – гормон роста, цитокины и соматомедины.
Все они влияют на состояние организма в целом, и от баланса данных веществ в организме во многом зависит здоровье человека.
Разновидности гормонотерапии
Лечение гормонами может носить заместительный, стимулирующий и тормозящий характер.
Заместительная гормонотерапия назначается при таких патологиях, когда наблюдается частичное либо полное прекращение работы эндокринных желёз. Больной принимает препараты, в которых содержится сам недостающий гормон или его аналог, полученный химическим путём.
Особенность такого лечения заключается в необходимости регулярного поступления вещества в организм извне; в противном случае терапевтический эффект исчезает. По этой причине в большинстве случаев курс лечения длится всю жизнь пациента (лечащий врач может корректировать дозировку и заменять один препарат другим, опираясь на результаты анализов больного). Так, например, происходит при сахарном диабете или заболеваниях щитовидной железы.
Внимание: пациентам настоятельно рекомендуют строго соблюдать режим приёма гормональных препаратов, который должен быть адаптирован к физиологическим процессам организма.
Стимулирующая гормонотерапия показана в тех случаях, когда необходимо «запустить» деятельность эндокринной железы и выявить её потенциал. Такой вид лечения носит временный характер, а иногда проводится в несколько курсов с перерывами (например, для стимуляции работы надпочечников).
Тормозящая (блокирующая) гормонотерапия применима в тех ситуациях, когда железа производит гормон в чрезмерном количестве. Также данный вид лечения показан в борьбе с рядом новообразований. Суть метода заключается в поступлении в организм вещества, которое является антагонистом избыточного гормона, либо вещества, блокирующего излишнюю активность железы.
Как правило, тормозящую гормонотерапию используют как часть комплексного лечения при оперативном вмешательстве или химиотерапии, поскольку в качестве самостоятельного метода она недостаточно эффективна.
Гормональная терапия: какие заболевания лечит?
Несмотря на то, что тема лечения гормонами порождает множество споров в профессиональной медицинской среде, эффективность данного вида терапии научно доказана и подтверждена практикой.
Применение гормональных препаратов позволяет добиваться положительных результатов в борьбе с целым рядом заболеваний:
гипотиреозом и гипертиреозом;
сахарным диабетом (преимущественно первого типа, но иногда и второго);
гормонозависимыми опухолями репродуктивной системы;
злокачественными опухолями предстательной железы;
астмой, аллергическим ринитом и прочими патологиями, возникающими на фоне иммунной реакции на аллергены;
гормональным дисбалансом и прочими болезнями, вызванными нарушениями функции желёз.
Стоит отметить, что при тяжёлом проявлении симптомов менопаузы женщинам также нередко назначают терапию гормонами. Однако гормональные препараты дают положительный эффект в борьбе с хроническими и поддающимися лечению состояниями исключительно под наблюдением врача!
Нужна помощь? Обращайтесь в многопрофильную клинику «ДИАЛАЙН». У нас Вы пройдёте полное обследование, сдадите все необходимые анализы и получите заключение специалиста о состоянии Вашего здоровья. При необходимости мы предложим Вам пройти курс лечения и будем сопровождать Вас, вместе добиваясь положительного результата.
Рациональная глюкокортикоидная терапия бронхиальной астмы
Согласно рекомендациям современных руководств по бронхиальной астме (БА), основной группой препаратов, использующихся для превентивного лечения больных БА (за исключением легкой/интермиттирующей формы заболевания), являются ингаляционные глюкокортикоиды
Согласно рекомендациям современных руководств по бронхиальной астме (БА), основной группой препаратов, использующихся для превентивного лечения больных БА (за исключением легкой/интермиттирующей формы заболевания), являются ингаляционные глюкокортикоиды (ИГК) [1–3]. Первый из них — беклометазона дипропионат был внедрен в клиническую практику в 1972 г. и до сих пор находит широкое применение благодаря низкой стоимости и безопасности.
В настоящее время в лечении БА используют еще четыре препарата из группы ИГК: флютиказона пропионат, будесонид, триамцинолона ацетонид, флунизолид.
Несмотря на довольно длительную историю клинического применения глюкокортикоидов (ГК), терапия БА по-прежнему вызывает немало вопросов, в том числе:
В настоящем обзоре мы попытаемся провести анализ литературных данных и основных рекомендаций по назначению ГК больным БА.
В начале коротко о том, каковы современные представления о механизмах действия ГК при БА. Доказано, что ГК влияют на иммунные и воспалительные процессы дыхательных путей посредством индукции экспрессии различных генов. ГК также снижают количество и/или активность клеток воспаления (лимфоцитов, макрофагов, тучных клеток, эозинофилов), влияют на сосудистую проницаемость, отек слизистой оболочки, субэпителиальный фиброз, уменьшают продукцию слизи в бронхах, способствуют восстановлению поврежденного эпителия и т. д.
Маловероятно, чтобы при остром приступе БА эффект ГК был связан с супрессией образовавшихся цитокинов и клеток воспаления, инфильтрирующих дыхательные пути, поскольку для проявления таких механизмов действия требуется как минимум 6–72 ч [4, 5]. Скорее всего, высокая терапевтическая эффективность стероидов связана с восстановлением чувствительности β-адренорецепторов дыхательных путей, количество которых снижается в результате приема β2-агонистов и развития самого процесса воспаления [4, 5]. Показано, что однократное введение преднизолона в/в и даже ингалирование беклометазона предотвращает десенситизацию β2-адренорецепторов [5], хотя следует учесть также протективный эффект самих β-агонистов на тучные клетки и плазменную экссудацию сосудов [4, 5].
Комплементарность действия при комбинации ГК и b2-агонистов доказана на экспериментальном («эффект Эйкелберга»: β2-агонисты активируют глюкокортикоидные рецепторы, а стероиды повышают экспрессию гена β2-адренорецептора) [6], а также клиническом уровнях (при приеме комбинированного препарата симбикорта отмечено более быстрое наступление бронходилатации и улучшение шкалы симптомов БА, по сравнению с терапией будесонидом и формотеролом через отдельные ингаляторы) [7].
Показания к назначению ГК при бронхиальной астме
Назначение ГК показано в тех случаях, когда пациент испытывает потребность в ингаляционном β2-агонисте короткого действия один раз в день (Британское руководство по БА) [2] или 3 раза в нед (GINA) [1]. Терапию целесообразнее начинать с высоких доз ИГК, чтобы достичь адекватного контроля над астмой (минимум приступов, снижение тяжести заболевания, достижение нормальных/почти нормальных показателей функции легких с минимумом побочных эффектов лекарственных средств), с последующим снижением их дозы (принцип «step down») [1, 8].
Доказано, что раннее начало лечения ГК более эффективно предотвращает развитие воспалительного процесса и структурных изменений дыхательных путей, особенно у детей [9]. При приеме даже малых доз будесонида (100 мкг 2 раза в сут) у детей заметно улучшались показатели пикфлоуметрии, клиническая симптоматика, снижалась потребность в β-агонистах короткого действия, хотя для предотвращения постнагрузочного бронхоспазма им требовалась более высокая доза ИГК (400 мкг в сут) [9]. По последним данным, флютиказон способен приостанавливать воспалительный процесс, но при этом не влияет на структурные изменения дыхательных путей, т. е. на ремоделирование [10].
Важную роль при тяжелой форме БА играют не только подбор адекватной дозы необходимых антиастматических средств, но и правильное назначение системных ГК.
Назначение ГК per os показано:
Больным БА преднизолон следует назначать из расчета 1–2 мг/кг веса в сут сроком не более 10 дней, с постепенным снижением суточной дозы на фоне приема ИГК [11, 12].
По мнению американских экспертов (EPR-2), пероральный преднизолон в дозе 50 мг целесообразно назначать взрослым больным БА однократно в течение 15 ч: тем самым количество эозинофилов в бронхолегочной лаважной жидкости супрессируется более эффективно, чем при приеме препарата в другие часы (в 8 или 20 ч) [3].
При купировании тяжелого приступа БА доказана эквивалентность терапевтического действия ГК, назначаемых больным в/в и перорально [12–15]. Установлено, кроме того, что различий в изменении ОФВ1 у больных с острым тяжелым приступом БА, которым вводили метилпреднизолон в/в в дозах 60, 160 и 500 мг в сут, не существует; не удалось выявить также влияния на уровень ОФВ1 низких и высоких доз преднизолона (1 и 6 мг/кг веса), вводимых в/в каждые 6 ч больным БА, поступившим в отделение неотложной медицины [13–15].
По данным Nana и соавт. [16], через 1 нед после лечения тяжелых астматиков ингаляционным будесонидом в дозе 1600 мкг 2 раза в день (I группа) и таблетированным преднизолоном 40 мг (II группа) уровень ОФВ1 повысился в обеих группах в одинаковой степени — в среднем на 17%. Однако в группе пациентов, которым ГК назначали перорально, обострения болезни наблюдались в два раза чаще. В то же время лечение больного БА таблетированным преднизолоном обходится в 70 раз дешевле терапии таким современным ИГК, как флютиказон.
Показана эквивалентность терапевтической эффективности 1600 мкг будесонида и 5 мг таблетированного преднизолона у пациентов с БА [17].
Хотя при БА может быть достигнут доза-ответ на лечение ИГК, наращивание дозы стероида, как правило, не приводит к дальнейшему улучшению функции легких [18]. Более того, парадоксальным кажется полученное доказательство равной эффективности высоких и низких доз флютиказона (1000 и 100 мкг в сут) при 8-недельном лечении больных со впервые диагностированной легкой и средней степенью БА [19]. Тяжелая форма БА, как правило, требует применения высоких доз ИГК с самого начала терапии [20, 21].
Недопустимо использование в лечении больных БА депонированных ГК (дексаметазон, кеналог, полькортолон) из-за вызываемой ими выраженной супрессии надпочечниковой функции и невозможности назначения этих препаратов по альтернирующей схеме.
В англоязычной литературе последних лет появился термин «brittle asthma», при которой более выраженный, по сравнению с применением ГК, терапевтический эффект отмечается после подкожного введения таким больным тербуталина [20].
Продолжительность приема ГК
У больных БА такие проявления, как кашель, свистящее и затрудненное дыхание, уменьшаются через несколько дней после приема ИГК [21, 22]; значительное облегчение течения заболевания наблюдается спустя недели [14, 23], но для максимального улучшения бронхиальной гиперреактивности ИГК требуется принимать регулярно на протяжении нескольких месяцев и лет [24, 25].
У большинства пациентов с БА снижение дозы ИГК через несколько месяцев терапии, как правило, не приводит к ухудшению течения заболевания [24–26]. Однако уже спустя несколько недель после полной отмены ИГК могут появиться симптомы неконтролируемой БА [25, 26]. Поскольку улучшение бронхиальной гиперреактивности может быть достигнуто примерно через 6–8 нед после начала приема беклометазона (в суточной дозе 400–2000 мкг), чтобы избежать возникновения побочных эффектов, дозу ИГК в дальнейшем следует снижать [26, 27].
Стероид-резистентность
Стероид-резистентная астма (СРА) — это астма, при которой после 1–2-недельного приема преднизолона в дозе
40 мг в сут объем форсированного выдоха за 1 сек (ОФВ1) не повышается более чем на 15% в ответ на вдыхание β2-агониста [28].
Как правило, СРА страдают пациенты с тяжелой формой заболевания. Этиопатогенез СРА обусловлен различными факторами: снижение количества глюкокортикоидных рецепторов дыхательных путей и/или повышение концентрации альтернативной им формы типа β, изменение супрессии транскрипционных факторов, преобладание относительно резистентных к ГК нейтрофилов в бронхиальном пространстве, резко выраженные структурные изменения дыхательных путей и т. д. [29, 30]. Возможно, играет также роль инфицирование таких больных Chlamidia pneumoniae или вирусами [31].
Прежде чем БА считать стероид-резистентной, следует:
Альтернатива глюкокостероидной терапии
На фоне приема ряда препаратов возможно снижение дозы системных и ингаляционных форм ГК. Не доказан стероидсберегающий эффект кромонов и кетотифена.
Назначение ингаляционных глюкокортикоидов довольно часто (
78%) позволяет уменьшить дозу системных стероидов и даже полностью отменить их прием. Исследование Meijer et al. показало, что высокая доза флютиказона более эффективна в отношении улучшения бронхиальной гиперчувствительности, чем преднизолон, принимаемый перорально [34]. Стероидсберегающий эффект пульмикорта-турбухалера был подтвержден в ходе проведенного нами исследования [35]: у детей, находящихся в отделение интенсивной терапии, более ранний клинический и бронходилатирующий эффект (в течение первых 4 ч) был выявлен в случае использования будесонида в дозе 1600 мкг и тербуталина, по сравнению с группой больных, получавших лечение таблетированным преднизолоном в дозе 2 мг/кг веса и β2-агонистом.
У больных СРА уменьшение дозы или полное прекращение приема пероральных ГК становится возможным также благодаря назначению суспензии пульмикорта, вдыхаемого через небулайзер. Небулизированный пульмикорт — уникальный стероид, влияющий на функциональные показатели легких значительно быстрее других ГК, вводимых парентерально или перорально [35, 36]. В многоцентровом исследовании T. Higgenbottam и соавт. у 23 больных из 43 после 12 нед терапии небулизированным пульмикортом в дозе 2 мг в сут удалось снизить дозу таблетированного преднизолона на 59% от исходной дозы (p
Д. Ш. Мачарадзе, доктор медицинских наук
Детская городская поликлиника № 102, Москва
Оказание скорой медицинской помощи при острых аллергических заболеваниях
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
к.м.н. И.В. Сидоренко, профессор И.С. Элькис,
к.м.н. А.В. Тополянский, профессор А.Л. Верткин
Научный Центр здоровья детей РАМН, Москва
ММА имени И.М. Сеченова
МГМСУ им. Н.А. Семашко
Станция скорой и неотложной медицинской помощи, Москва
Национальное научно-практическое общество скорой медицинской помощи, Москва
П о данным Национального научно–практического общества скорой медицинской помощи, за последние 3 года число вызовов по поводу острых аллергических заболеваний в целом по РФ возросло на 18%. При этом их частота в разных регионах составляет от 1 до 5% всех случаев выездов бригад скорой медицинской помощи.
Основные причины возникновения и патогенез
Патогенез аллергических реакций изучен на сегодняшний день достаточно полно и подробно описан во многих отечественных и зарубежных монографиях по аллергологии и клинической иммунологии. В любом случае в ткани шокового органа или органа–«мишени», которым могут быть кожа, бронхи, желудочно–кишечный тракт и т.д., появляются признаки аллергического воспаления. Центральная роль в реализации этих иммунопатологических реакций принадлежит иммуноглобулинам класса Е (IgE), связывание которых с антигеном приводит к выбросу из тучных клеток медиаторов аллергии (гистамина, серотонина, цитокинов и др.).
Наиболее часто аллергические реакции развиваются при воздействии ингаляционных аллергенов жилищ, эпидермальных, пыльцевых, пищевых аллергенов, лекарственных средств, антигенов паразитов, а также при ужалении и укусах насекомых. Лекарственная аллергия наиболее часто развивается при применении анальгетиков, сульфаниламидов и антибиотиков из группы пенициллинов, реже цефалоспоринов. Кроме того, высока частота развития латексной аллергии.
Клиническая картина, классификация и диагностические критерии
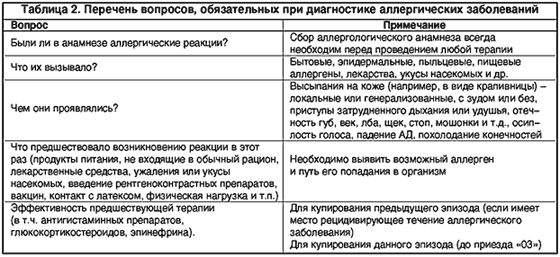
С точки зрения оказания помощи и оценки прогноза острые аллергические заболевания можно классифицировать следующим образом (табл. 1):
Легкие – аллергический ринит (круглогодичный или сезонный), аллергический конъюнктивит (круглогодичный или сезонный), крапивница.
Средней тяжести и тяжелые – генерализованная крапивница, отек Квинке, острый стеноз гортани, среднетяжелое обострение бронхиальной астмы, анафилактический шок.
Наибольшую настороженность при оказании медицинской помощи на догоспитальном этапе должны вызывать прогностически неблагоприятные случаи развития у пациентов жизнеугрожающих состояний: тяжелый приступ астмы (status asthmaticus), анафилактический шок, отек Квинке в области гортани, острый стеноз гортани.
При анализе клинической картины аллергической реакции врач скорой медицинской помощи должен получить ответы на вопросы, представленные в таблице 2.
При начальном осмотре следует оценить наличие: стридора, диспноэ, свистящего дыхания, одышки или апноэ; гипотензии или синкопе; изменений на коже (высыпаний по типу крапивницы, отеков Квинке, гиперемии, зуда); гастроинтестинальных проявлений (тошноты, болей в животе, диареи); изменений сознания. Если у больного стридор, выраженная одышка, гипотензия, аритмия, судороги, потеря сознания или шок, то данное состояние рассматривается как жизнеугрожающее.
Лечение острых аллергических заболеваний
При острых аллергических заболеваниях на догоспитальном этапе неотложная терапия строится по направлениям:
Прекращение дальнейшего поступления в организм предполагаемого аллергена. Например, в случае реакции на лекарственный препарат, введенный парентерально или при укусе/ужалении насекомых – наложение жгута выше места инъекции или укуса на 25 мин (каждые 10 минут необходимо ослаблять жгут на 1–2 минуты); к месту инъекции или укуса – лед или грелка с холодной водой на 15 мин; обкалывание в 5–6 точках и инфильтрация места инъекции или укуса 0,3 – 0,5 мл 0,1% раствором эпинефрина с 4,5 мл изотонического раствора хлорида натрия.
Противоаллергическая терапия (антигистаминные препараты или глюкортикостероиды). Введение антигистаминных препаратов показано при аллергическом рините, аллергическом конъюнктивите, крапивинице. Терапию глюкокортикоидами (ГКС) проводят при анафилактическом шоке и при отеке Квинке (в последнем случае – препарат выбора): внутривенно вводят преднизолон (взрослым – 60–150 мг, детям – из расчета 2 мг на 1 кг массы тела). При генерализованной крапивнице или при сочетании крапивницы с отеком Квинке высокоэффективен бетаметазон 1–2 мл внутримышечно. При отеке Квинке для предупреждения влияния на ткани гистамина необходимо комбинировать антигистаминные препараты нового поколения (лоратадин) с глюкокортикоидами.
Симптоматическая терапия. При развитии бронхоспазма – показано ингаляционное введение b 2–агонистов и других бронхолитических и противовоспалительных препаратов через небулайзер. Коррекцию артериальной гипотонии и восполнение объема циркулирующей крови проводят с помощью введения солевых и коллоидных растворов (изотонического раствора хлорида натрия 500–1000 мл, гидроксиэтилированного крахмала 500 мл, полиглюкина 400 мл). Применять вазопрессорные амины (допамин 400 мг на 500 мл 5% глюкозы, норадреналин 0,2 – 2 мл на 500 мл 5% раствора глюкозы; доза титруется до достижения уровня систолического давления 90 мм рт.ст.) можно только после восполнения объема циркулирующей крови. При брадикардии возможно введение атропина в дозе 0,3–0,5 мг подкожно (при необходимости введение повторяют каждые 10 минут). При наличии цианоза, диспноэ, сухих хрипов показана также кислородотерапия.
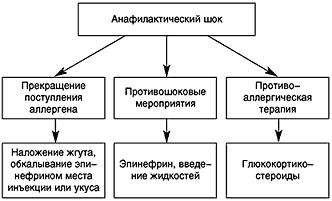
Противошоковые мероприятия (рис. 1). При анафилактическом шоке больного следует уложить (голова ниже ног), повернуть голову в сторону (во избежание аспирации рвотных масс), выдвинуть нижнюю челюсть, удалить съемные зубные протезы. Подкожно вводят эпинефрин в дозе 0,1 – 0,5 мл 0,1% раствора (препарат выбора), при необходимости инъекции повторяют каждые 20 минут в течение часа под контролем уровня АД. При нестабильной гемодинамике с развитием непосредственной угрозы для жизни возможно внутривенное введение эпинефрина. При этом 1 мл 0,1% раствора эпинефрина разводится в 100 мл изотонического раствора хлорида натрия и вводится с начальной скоростью 1 мкг/мин (1 мл в мин). При необходимости скорость может быть увеличена до 2–10 мкг/мин. Внутривенное введение эпинефрина проводится под контролем частоты сердечных сокращений, дыхания, уровня АД (систолическое артериальное давление необходимо поддерживать на уровне более 100 мм рт.ст. у взрослых и > 50 мм рт.ст. у детей). Лекарственные средства, применяемые при аллергических заболеваниях различной степени тяжести и их эффективность представлены в таблице 3.
Рис. 1. Алгоритм лечения анафилактического шока
Клиническая фармакология лекарственных средств, применяемых для лечения острых аллергических заболеваний
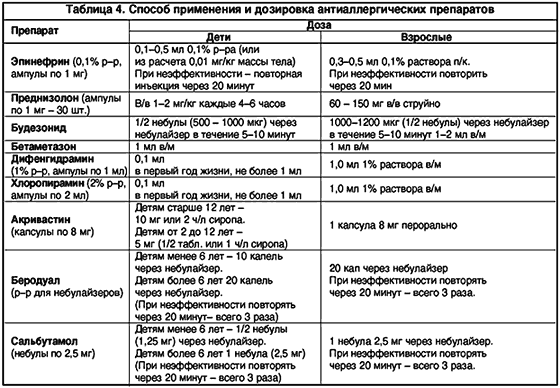
Способ применения и дозировка антиаллергических препаратов представлены в таблице 4.
Эпинефрин является прямым стимулятором a – и b –адренорецепторов, что обусловливает все его фармакодинамические эффекты. Механизм противоаллергического действия реализуется:
Способ применения и дозировка антиаллергических препаратов представлены в таблице 4.Эпинефрин является прямым стимулятором – и –адренорецепторов, что обусловливает все его фармакодинамические эффекты. Механизм противоаллергического действия реализуется:
• стимуляцией a –адренорецепторов, сужением сосудов органов брюшной полости, кожи, слизистых оболочек, повышением артериального давления;
• положительным инотропным действием (увеличивается сила сердечных сокращений за счет стимуляции b 1–адренорецепторов сердца);
• стимуляцией b 2–адренорецепторов бронхов (купирование бронхоспазма);
• подавлением дегрануляции тучных клеток и базофилов (за счет стимуляции внутриклеточной цАМФ).
При парентеральном введении препарат действует непродолжительно (при внутривенном – 5 мин, при подкожном – до 30 мин), так как быстро метаболизируется в окончаниях симпатических нервов, в печени и других тканях с участием моноаминооксидазы (МАО) и катехол–О–метилтрансферазы (КОМТ).
Побочные эффекты: головокружение, тремор, слабость; сильное сердцебиение, тахикардия, различные аритмии (в том числе желудочковые), появление болей в области сердца; затруднение дыхания; увеличение потливости; чрезмерное повышение артериального давления; задержка мочи у мужчин, страдающих аденомой предстательной железы; повышение уровня сахара в крови у больных сахарным диабетом. Описаны также некрозы тканей при повторном подкожном введении в одно и то же место вследствие местного сужения сосудов.
Противопоказания: артериальная гипертензия; выраженный церебральный атеросклероз либо органическое поражение головного мозга; ишемическая болезнь сердца; гипертиреоз; закрытоугольная глаукома; сахарный диабет; гипертрофия предстательной железы; беременность. Однако даже при этих заболеваниях возможно назначение эпинефрина при анафилактическом шоке по жизненным показаниям и под строгим врачебным контролем.
Механизм противоаллергического действия глюкокортикоидов основан на следующих эффектах:
• иммунодепрессивное свойство (подавление роста и дифференцировки иммунных клеток – лимфоцитов, плазмоцитов, уменьшение продукции антител);
• предупреждение дегрануляции тучных клеток и выделения из них медиаторов аллергии;
• уменьшение проницаемости сосудов, повышение артериального давления, улучшение бронхиальной проходимости.
Для парентерального введения при проведении неотложной терапии на догоспитальном этапе применяется преднизолон. Для лечения бронхиальной астмы, аллергического ринита, аллергического конъюнктивита разработаны топические формы глюкокортикостероидов (флутиказон, будезонид). Побочные эффекты системных ГКС: артериальная гипертензия, возбуждение, аритмия, язвенные кровотечения. Побочные эффекты топических ГКС: осиплость голоса, нарушение микрофлоры с дальнейшим развитием кандидоза слизистых, при применении высоких доз – атрофия кожи, гинекомастия, прибавка массы тела и др. Противопоказания: язвенная болезнь желудка и 12–перстной кишки, тяжелая форма артериальной гипертензии, почечная недостаточность, повышенная чувствительность к глюкокортикоидам в анамнезе.
Бетаметазон – глюкокортикостероидный препарат, состоит из 2 мг динатрия фосфата и 5 мг дипропионата бетаметазона. Бетаметазона динатрия фосфат обеспечивает быстроту наступления эффекта. Пролонгированное действие обеспечивается за счет бетаметазона дипропионата. Препарат оказывает иммунодепрессивное, противоаллергическое, десенсибилизирующее и противошоковое действие. Бетаметазон биотрансформируется в печени. Доза препарата зависит от степени тяжести заболевания и клинической картины течения. Применяется для лечения острых аллергических заболеваний в виде внутримышечных инъекций по 1–2 мл. При однократном введении существенных побочных действий не отмечено.
Антигистаминные средства (блокаторы Н1–гистаминовых рецепторов)
Существует несколько классификаций антигистаминных препаратов. Согласно одной их них, выделяют препараты первого, второго и третьего поколения (при этом до сих пор дискутируется вопрос о принадлежности разных препаратов ко 2–му или 3–му поколению). В другой, более популярной среди клиницистов классификации, выделяют классические антигистаминные препараты, например, хлоропирамин, и препараты нового поколения (акривастин, фексофенадин, лоратадин и др.)
Необходимо отметить, что для классических антигистаминных препаратов, в отличие от препаратов нового поколения, характерной является короткая продолжительность действия при относительно быстром наступлении клинического эффекта. Многие из них имеются в парентеральных формах. Все это определяет широкое использование классических антигистаминных средств и в настоящее время.
Хлоропирамин – один из широко применяемых классических антигистаминных препаратов. Обладает значительной антигистаминной активностью, периферическим антихолинергическим и умеренным спазмолитическим действием. При приеме внутрь быстро и полностью абсорбируется из ЖКТ. Максимальная концентрация в крови достигается в течение первых 2 часов, терапевтический уровень концентрации сохраняется 4–6 часов. Эффективен в большинстве случаев для лечения сезонного и круглогодичного аллергического ринита и конъюнктивита, крапивницы, атопического дерматита, экземы; в парентеральной форме – для лечения острых аллергических заболеваний, требующих неотложной помощи. Обладает широким диапазоном используемых терапевтических доз. Не накапливается в сыворотке крови, поэтому не вызывает передозировки при длительном применении. Для препарата характерно быстрое наступление эффекта и небольшая продолжительность (в том числе и побочного) действия. Может комбинироваться с другими Н1–блокаторами с целью увеличения продолжительности противоаллергического действия. Выпускается в таблетках и в ампулах для внутримышечного и внутривенного введения.
Антигистаминные препараты нового поколения лишены кардиотоксического действия, конкурентно влияют на гистамин, не метаболизируются печенью (например, фармакокинетика акривастина не меняется даже у больных с нарушенными функциями печени и почек) и не вызывают тахифилаксии.
Акривастин – препарат с высокой антигистаминной активностью при минимально выраженном седативном и антихолинергическом действии. Особенностью его фармакокинетики является низкий уровень метаболизма и отсутствие кумуляции и привыкания. Акривастин предпочтителен в случае, когда нет необходимости постоянного противоаллергического лечения. Желатиновая капсула быстро всасывается в желудке, обеспечивая быстрое наступление эффекта. Препарат обладает коротким периодом действия, что позволяет использовать гибкий режим дозирования. Нет кардиотоксического действия. Селективно влияя на Н1–рецепторы, не раздражает слизистую желудка. Нет воздействия на Н2–рецепторы.
Лоратадин – антигистаминный препарат нового поколения безрецептурного отпуска.
Показания к применению: аллергический ринит (сезонный и круглогодичный), аллергический конъюнктивит, крапивница, генерализованная крапивница, отек Квинке, аллергические реакции на укусы насекомых, зудящие дерматозы (контактные аллергодерматиты, хронические экземы).
У препарата отсутствуют такие побочные эффекты, как сонливость, сухость во рту, головная боль, головокружение.
Бронхоспазмолитики: b 2–агонисты короткого действия и холинолитики
Беродуал – комбинированный бронхоспазмолитический препарат, содержащий два бронхорасширяющих вещества: фенотерол ( b 2–агонист) и ипратропиум бромид (холинолитик). Одна доза беродуала содержит 0,05 мг фенотерола и 0,02 мг ипратропиума бромида.
Сальбутамол – селективный агонист b 2– адренорецепторов. Бронхорасширяющий эффект сальбутамола наступает через 4–5 минут. Действие препарата постепенно возрастает до своего максимума к 40–60 минуте. Период полувыведения 3–4 часа, продолжительность действия – 4–5 часов.
Способ применения: с помощью небулайзера; небулы по 2,5 мл, содержащая 2,5 мг сальбутамола в физиологическом растворе. Назначаются 1–2 небулы (2,5–5,0 мг) на ингаляцию в неразбавленном виде. Если улучшения не наступает, проводят повторные ингаляции по 2,5 мг каждые 20 мин. в течение часа.
Типичные ошибки в применении лекарственных средств при лечении острых аллергических заболеваний на догоспитальном этапе
• Изолированное назначение Н1–гистаминовых блокаторов при тяжелых аллергических реакциях, равно как и при бронхообструктивном синдроме, не имеет самостоятельного значения и на догоспитальном этапе лишь приводит к неоправданной потере времени.
• Использование дипразина опасно еще и усугублением гипотонии.
• Позднее назначение ГКС; необоснованное применение малых доз ГКС.
• Использование отдельных препаратов, не показанных для лечения аллергических заболеваний (глюконата кальция, хлористого кальция и пр.).
• Наличие в табеле оснащения бригад скорой помощи препаратов однонаправленного действия экономически неоправданно.
• Неиспользование топических ГКС и b 2–агонистов при аллергическом стенозе гортани и бронхоспазме.
Больные с тяжелыми аллергическими заболеваниями должны быть обязательно госпитализированы. При легких аллергических заболеваниях вопрос о госпитализации решается в каждом случае индивидуально.
ПРИЛОЖЕНИЕ
Аллергический стеноз верхних дыхательных путей у детей
Основные причины возникновения и патогенез
Синдром обструкции верхних дыхательных путей (круп, острый стенозирующий ларинготрахеит) у детей – одна из частых причин обращения за неотложной помощью. Выделяют острый аллергический стеноз гортани и стеноз, развивающийся на фоне ОРВИ.
Основной причиной развития аллергического стеноза верхних дыхательных путей с преимущественной локализацией процесса в области гортани является сенсибилизация организма к пищевым и лекарственным аллергенам, а также к аллергенам микроклещей домашней пыли (Dermatophagoides pteronyssinus и Dermatophagoides farinae), животных и др.
Острый аллергический стеноз верхних дыхательных путей чаще наблюдается у детей с наследственным предрасположением к аллергии. Развитию крупа нередко предшествует появление симптомов кожной и респираторной аллергии. Благоприятствуют возникновению аллергического стеноза гортани и такие анатомические особенности этого органа у детей, как мягкость хрящевого скелета, короткое и узкое преддверье и высоко расположенная гортань, наличие нежной, богатой клеточными элементами слизистой оболочки и рыхлого, с обильной сосудистой сетью и большим количеством тучных клеток подслизистого слоя. Указанные особенности строения слизистой и подслизистой оболочек особенно характерны для окруженного плотным перстневидным хрящом участка гортани. Эта область проецируется на подсвязочное пространство, в ней и развивается у детей максимально выраженный отек. Чаще круп развивается у детей в возрасте от 6 месяцев до 3 лет, при этом мальчики страдают им в 3–4 раза чаще, чем девочки.
Патогенетическую основу аллергического стеноза верхних дыхательных путей составляют IgЕ–опосредуемые аллергические реакции, вызывающие развитие в слизистой оболочке гортани воспаления в виде отека, гиперсекреции слизи, спазма гладкой мускулатуры верхних дыхательных путей; у отдельных больных возникает также бронхоспазм. Развитие острого стенозирующего ларинготрахеита может быть связано и с воздействием вирусной инфекции, химических поллютантов, изменением метеоситуации.
Клиническая картина, классификация и диагностические критерии
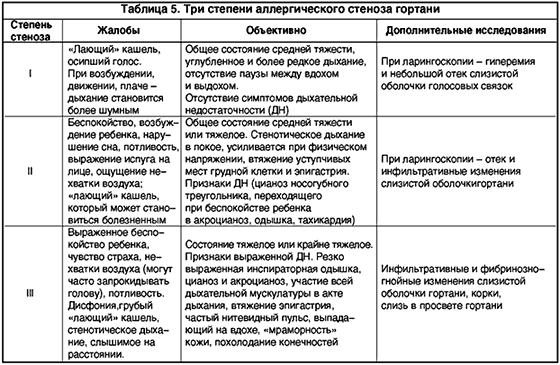
Острый стеноз гортани является причиной развития дыхательной недостаточности и нарушения общего состояния ребенка. Различают три степени стеноза в зависимости от выраженности сужения гортани:
I степень стеноза гортани – компенсированный стеноз;
II степень – субкомпенсированный стеноз;
III степень – декомпенсированный стеноз (табл. 5).
У детей с аллергическим стенозом гортани обычно выявляют отягощенную аллергическими реакциями и заболеваниями наследственность, нередко у них отмечаются также проявления атопического дерматита, пищевой и лекарственной аллергии. Для этого варианта крупа характерно внезапное развитие стеноза «на фоне полного здоровья», при отсутствии катаральных явлений, нормальной температуре тела, а также сравнительно быстрое купирование симптомов болезни при назначении адекватной терапии. У ряда детей одновременно с проявлениями аллергического стеноза гортани развивается бронхообструктивный синдром.
Острый стеноз гортани, развивающийся на фоне острой респираторной инфекции, характеризуется более постепенным началом болезни, возникновением стеноза на фоне катаральных явлений со стороны верхних дыхательных путей, повышением температуры, развитием симптомов интоксикации, воспалительных изменений в общем анализе крови.
Стеноз гортани необходимо дифференцировать с дифтерией гортани, инородным телом дыхательных путей, обструктивным бронхитом, заглоточным абсцессом, бронхиальной астмой, коклюшем, пневмонией с проявлениями дыхательной недостаточности.
Лечение острого стеноза гортани
Дети с острым стенозом гортани подлежат обязательной госпитализации. Проводимая при остром стенозе гортани терапия должны быть патогенетической и направленной на восстановление воздушной проходимости верхних дыхательных путей. Лечение проводится с учетом выраженности стеноза гортани, начинается бригадами СМП на вызове, продолжается по пути следования в стационар. Время оказания догоспитальной помощи больному не должно превышать 60 минут.
Для лечения острого стеноза гортани в компенсированной стадии (I степень) на догоспитальном этапе используются ингаляции глюкокортикостероидов (будезонида через небулайзер в дозе 0,25 мг, при неэффективности или отсутствии небулайзеров применяются антигистаминные препараты: в/м (хлоропирамин, 2%–ный раствор, 0,1 мл в первый год жизни) или перорально (для детей от 12 лет – акривастин (7 мг, капсула) или лоратадин 10 мг (1 табл. или 2 чайных ложки сиропа).
Терапия острого стеноза гортани в стадии неполной компенсации (II степень) начинается с ингаляций глюкокортикостероидов через небулайзер в дозе 0,5 мг. При неэффективности проводят повторные ингаляции будезонида в той же дозе через небулайзер с интервалом в 20 минут (максимально 3 раза).
При отсутствии небулайзеров применяются антигистаминные препараты (хлоропирамин в/м), системные глюкокортикостероиды (преднизолон из расчета 2 мг/кг). При недостаточном эффекте дополнительно назначается подкожное введение 0,1 % раствора эпинефрина из расчета 0,01 мг/кг массы тела.
Стеноз гортани III степени протекает с проявлениями дыхательной и сердечно–сосудистой недостаточности, нарушением метаболических процессов, признаками токсикоза, что обусловливает необходимость немедленной госпитализации. На догоспитальном этапе лечение стеноза гортани III степени также начинается с ингаляций глюкокортикостероидов через небулайзер в дозе 1 мг.
При возникновении бронхообструктивного синдрома лечение проводится растворами b 2–агонистов короткого действия (беродуала по 10–20 капель детям до 6 лет или сальбутамола – 1/2–1 небула детям старше 6 лет) через небулайзер.