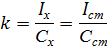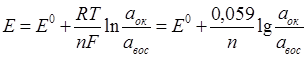Техническая гальванопластика
Гальванопластика — направление прикладной электрохимии, направленное на создание изделий путем электрохимического осаждения металлов и сплавов на различные носители формы (формообразующие элементы) в жидких средах.
Принцип формирования металлического осадка на поверхности модели, такой же как и при гальваническом нанесении покрытий, но в отличии от классической гальваники (гальваностегии) – толщина формируемых металлических осадков может достигать нескольких сантиметров.
В первой половине 20 века применение гальванопластики с целью получения технических изделий превратилось в полноценную промышленную технологию получения сложных и точных изделий.
Правила построения градуировочного графика при фотометрическом анализе
Фотометрический анализ при контроле гальванических электролитов применяется для определения малых концентраций добавок и примесей, титриметрический анализ которых затруднён или нецелесообразен.
Распространёнными фотометрическими измерениями являются определения:
• солей хрома III в электролите хромирования и растворе хромитирования,
• общего кобальта и никеля в электролитах твёрдого золочения, серебрения и нанесения сплава «Никель-Кобальт»,
• висмута в электролите нанесения сплава «Олово-Висмут»,
• определение палладия в активаторе для металлизации диэлектриков,
• определение примесей меди, железа и никеля в различных электролитах,
• а также турбидиметрическое определение сульфатов в электролите хромирования и в сульфаматных электролитах для определения степени гидролиза сульфаматов и пр.
Физико-химические методы анализа основаны на взаимосвязи между составом системы и ее физическими и физико-химическими свойствами. Функциональная зависимость между численным значением данного физического или физико-химического свойства и содержанием анализируемого вещества может быть выражена графиком или формулой.
Основой для построения градуировочного графика является приготовление стандартных растворов.
Стандартные растворы необходимо готовить из аттестованных государственных образцов (ГСО). Если таковых не имеется, необходимо четко придерживаться основных требований к точности приготовления стандартных растворов:
• следует применять соединения квалификации не ниже ч.д.а;
• использование реактивов с просроченным сроком годности недопустимо;
• для приготовления стандартных растворов использовать только гостированную мерную посуду.
Особое внимание обратить на условия и сроки хранения растворов с содержанием вещества 1 мг/см3 хранят 1 год, 0,1 мг/см3 – 3 месяца (если нет других указаний, а также если нет помутнения, хлопьев, осадка), растворы с меньшим содержанием применяются свежеприготовленными. Стандартные растворы фильтровать не допускается.
Для определения содержания вещества методом градуировочного графика готовят 3 серии шкал стандартов. Указания по приготовлению шкалы стандартов конкретно оговорены в каждой методике.
При приготовлении параллельных шкал рабочие растворы готовят соответствующим разбавлением основного стандартного раствора, который готовится из одной взятой навески или ГСО.
Градуировочный график строят на миллиметровой бумаге или в электронной форме при помощи Excel, откладывая на оси абсцисс, указанную в методике определения концентрацию, а по оси ординат – измеренные значения оптической плотности.
Количественное значение оптической плотности для каждой точки градуировочного графика определяется как среднее арифметическое результатов параллельных измерений 3-х шкал.
С целью уменьшения погрешности графического измерения, необходимо подобрать такой масштаб графика, чтобы угол его наклона приблизительно равнялся 45º.
Градуировочный график должен нести следующую информацию:
• НД на метод проведения исследования;
• марка КФК, его заводской номер;
• длина рабочей грани кюветы;
• раствор сравнения (растворитель, нулевой раствор и т.д.), т.е. относительно чего снимались показания испытуемого раствора;
• на графике должны присутствовать данные 3-х параллельных измерений и среднее арифметическое значение (в виде таблицы).
Градуировочный график строится один раз в год и после ремонта прибора. Поверка графика должна проводиться 1 раз в квартал (если нет других указаний в методике определения), а также после приготовления реактивов из новой партии, поверки прибора. Поверка проводится по 3-м точкам графика наиболее часто встречающихся в работе концентраций. Данные поверки заносятся в журнал поверок градуировочных графиков или наносятся на обратную сторону графика в виде таблицы.
Несмотря на простоту и удобство, практическое использование градуировочных графиков в ряде случаев вносит дополнительную погрешность при определении концентрации растворов как за счет субъективного построения графической зависимости, так и за счет несоответствия графичеких (масштабных) погрешностей и погрешностей измерения оптических плотностей. Поэтому для получения более объективных результатов в фотометрическом анализе целесообразно построение градуировочного графика методом регрессивного анализа (уравнение регрессии).
Описание метода наименьших квадратов и пример построение уточнённого градуировочного графика на примере фотометрического определения железа – здесь.
Дополнение для приборов, имеющих стрелочное регистрирующее устройство:
На многих предприятиях до сих пор в эксплуатации находятся приборы, при работе на которых значение измеренного пропускания отсчитывают по стрелочному прибору. Эти устройства являются обычным источником погрешности именно при отсчитывании показаний. Для правильно сконструированного стрелочного прибора погрешность при отсчёте будет постоянной и, возможно, равной толщине стрелки, которая соответствует определённому отсчёту по шкале прибора. При допущении, что отсчёты пропускания, полученные каждым таким устройством, имеют постоянную недостоверность (обусловленную изменением мощности источника света, характеристиками детектора, электрическими шумами, положением кюветы, и обычно приводящую к суммарной погрешности от 0,2 до 1%), можно рассчитать погрешность, которую вызовет ненадёжность при регистрации концентрации определяемых частиц.
Для расчёта концентрационной погрешности необходимо изучить влияние недостоверности измерения пропускания на вычисленное значение концентрации. Для этого запишем закон Бера в форме, которая показывает, что зависимость от концентрации является экспоненциальной:
T = P/P0 = 10-abC, где (1)
b– толщина поглощающего слоя раствора в кювете,
С – концентрация оптически активного вещества,
а – удельная поглощательная способность, зависящая от природы вещества.
Из графика этой зависимости на рисунке можно определить, какое влияние на рассчитанное значение С окажет постоянная погрешность в пропускании.
Сначала рассмотрим спектрофотометрическое измерение раствора с низкой концентрацией (С1) определяемых частиц. Согласно рисунку этот раствор будет иметь высокое значение пропускание (Т1). Допуская, что недостоверность при отсчёте стрелочного прибора соответствует постоянной абсолютной погрешности в Т, можно определить из рисунка результирующую погрешность в определение С. Из экстраполирования линии видно, что абсолютная погрешность в концентрации (ΔС1) мала, когда раствор имеет высокое пропускание. Однако поскольку сама концентрация (С1) мала, относительная погрешность в концентрации (ΔС1/С1) довольно велика.
Теперь рассмотрим случай, когда имеется высокая концентрация (С2) определяемого вещества. Этот раствор будет иметь относительно низкое значение пропускания (Т2). Если снова допустить наличие постоянной погрешности в Т, то получим большую абсолютную погрешность (ΔС2) в концентрации, и хотя концентрация велика, относительная погрешность (ΔС2/С2) также будет велика.
Эти результаты свидетельствуют, что где-то между экстремальными значениями концентрации в пробах, имеющих высокие и низкие пропускания, должно существовать значение пропускания, для которого относительная погрешность в концентрации (ΔС/С) минимальна. В действительности относительная погрешность минимальна при 36,8%-ном пропускании. К этому выводу можно прийти и расчётным путём, вспомнив определение понятия поглощения:
А = lg (1/T) = 1/2,303 ln(1/T) = 0,434 ln (1/T) (2)
Если это уравнение продифференцировать относительно Т, то получим
Для того чтобы оценить относительную погрешность в значении поглощения и тем самым в концентрации, необходимо разделить каждую часть уравнения (3) на поглощение (А). Тогда
dA/А = (-0,434/TА) dT= (0,434/TlgT) dT (4)
Чтобы найти относительную погрешность в концентрации, заменим в этом уравнении А соответствующей величиной согласно закону Ламберта-Бера (1):
d(abC)/abC = (ab)dC/abC = dC/C = (0,434/T lgT) dT (5)
Уравнение (5) показывает, что относительная погрешность в концентрации (dC/C) непосредственно зависит от абсолютной недостоверности в пропускании (dT), а также от обратной величины произведения (TlgT), включающего значение самого пропускания. Графическая зависимость этого уравнения, показывающая относительную погрешность в концентрации (dC/C) как функцию пропускания (в %) при постоянной погрешности в отсчёте (dT), равной 1%, показана на рисунке:
Из рисунка видно, что относительная погрешность в концентрации достаточно низка при пропусканиях между 20 и 70%, но при переходе к очень низким или высоким значениям пропускания погрешность резко возрастает. Можно найти минимальную относительную погрешность в концентрации путём дифференцирования уравнения (5) и приравнивая выражения к нулю. Как указано ранее, минимальная погрешность имеет месть при 36,8%-ном пропускании или при поглощении, равном 0,434. Поэтому для спектрофотометров, имеющих стрелочное регистрирующее устройство, можно проводить измерение с наименьшей погрешностью, если отсчёты по шкале ограничены пределом от 20% до 70% пропускания (или от 0,7 до 0,2 единиц поглощения), а в оптимальном случае эти расчёты приближаются к значениям 36,8% пропускания или к 0,434 единиц поглощения. Обычно можно соблюдать эти ограничения путём соответствующего выбора толщины поглощающего слоя пробы (b) или путём разбавления раствора пробы, взятого для анализа.
Приведённые выше рассуждения применимы только к измерениям на спектрофотометрах, имеющих постоянную погрешность, связанную с отсчётом пропускания. Современные приборы обладают цифровой регистрацией, погрешность отсчёта не является для них фактором, лимитирующим правильность.
1) Переярченко П.В., Афанасьева О.Л., Замковая Л.А., Махоня Т.В., Гольнева Л.Н. Информационное письмо о правилах построения градуировочных графиков при фотоколориметрических методах исследования.
2) Петерс Д., Хайес Дж., Хифтье Г. Химическое разделение и измерение. Теория и практика аналитической химии. – М.: «Химия», 1978. – 816 с.
3) Булатов М.И., Малинкин И.П. Практическое руководство по фотометрическим методам анализа, Ленинград, Химия, 1986;
4) Справочник по физико-химическим методам исследования объектов окружающей среды под редакцией Арановича Г.И., Ленинград, Судостроение, 1979;
5) Новиков Ю.В., Ласточкина К.О., Болдина З.Н. Методы исследования качества воды водоемов, Москва, Медицина, 1990;
6) ГОСТ 4212–76 «Реактивы. Методика приготовления растворов для колориметрического, нефелометрического и других видов анализа».
Метод градуировочного графика
Метод градуировочного графика – это приём нахождения неизвестной концентрации (Сх) по величине аналитического сигнала пробы с помощью градуировочного графика. В аналитических определениях чаще всего имеют дело с прямолинейной градуировочной зависимостью. Уравнение прямой имеет вид y = a + bx, где у – аналитический сигнал, х – концентрация (может быть логарифм концентрации), коэффициент а – отрезок, отсекаемый прямой на оси ординат, коэффициент b –тангенс угла наклона прямой.
На практике устанавливают градуировочную зависимость путем измерения аналитического сигнала в стандартных растворах. Для проведения анализа необходимо иметь исходный стандартный раствор, который готовят по точной навеске, растворённой в мерной колбе. Если стандартный раствор нельзя приготовить по точной навеске, готовят раствор приблизительной концентрации, а затем устанавливают его концентрацию другим методом анализа. Концентрацию исходного стандартного раствора рассчитывают с четырьмя значащими цифрами.
Из исходного стандартного раствора, то есть точно известной концентрации, путем разбавления приготавливают серию стандартных растворов. Во всех приготовленных стандартных растворах измеряют аналитический сигнал. Строят график зависимости аналитического сигнала Ас i от концентрации определяемого компонента С i.
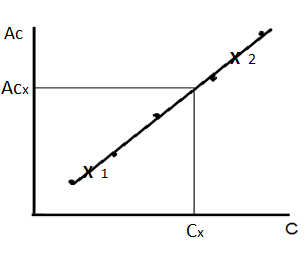
Затем измеряют аналитический сигнал в анализируемой пробе, строго соблюдая те же условия определения и режим работы прибора, как в стандартных растворах. По градуировочному графику находят концентрацию определяемого компонента в анализируемом растворе (рисунок 1.1). Более точные результаты получают, если для линейного участка градуировочного графика выводят уравнение Ас = a + b С и по нему рассчитывают концентрацию определяемого компонента.
Если измеренный аналитический сигнал превышает верхний предел линейной области графика, то анализируемый раствор разбавляют и повторяют измерения. Необходимую степень разбавления анализируемого раствора выбирают таким образом, чтобы концентрация определяемого компонента в разбавленном растворе и, соответственно, аналитический сигнал попадали в линейную область.
Рисунок 1.1 – Метод градуировочного графика
Построение градуировочного графика Ас = f (С) на миллиметровой бумаге проводят в следующем порядке:
1. Выбирают масштаб с учетом ошибки измерения и отмечают на осях координат ряд чисел, характеризующих масштаб. Значения концентрации С откладывают на оси абсцисс, а значения аналитического сигнала Ас – на оси ординат, указывают единицы измерения физических величин. Экспериментальные значения величин на осях координат откладывать не следует.
2. В координатах Ас – C наносят экспериментальные точки, полученные после измерения Ас в стандартных растворах.
3. Рассчитывают значения коэффициентов a и b для уравнения графика y = a + bx и коэффициент корреляции r, используя данные измерений в стандартных растворах (y = Aci, x = Ci). Расчёт проводят методом наименьших квадратов на компьютере (например, в программе Exel) или по формулам [1, c.48]. Записывают уравнение Ас = a + b С, подставив найденные значения коэффициентов a и b.
Коэффициент корреляции r отражает корреляцию параметров Ас и С:
– если r близок к единице (r ≥ 0,99), то корреляция характеризует между Ас и С количественную зависимость;
– если r ≈ 0,95, то зависимость считается полуколичественной;
– если r ≈ 0,90 и ниже, то зависимость считается качественной.
Метод стандартов
Метод стандартов – это расчётный приём нахождения неизвестной концентрации. Он имеет две разновидности.
Метод одного стандарта. Для проведения анализа готовят один стандартный раствор с концентрацией определяемого вещества Сст. Затем измеряют величины аналитического сигнала этого раствора (Iст ) и анализируемой пробы ( Ix ) в одинаковых условиях.
Из выражения для k выводим формулу для расчёта неизвестной концентрации:
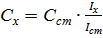
Метод двух стандартов (ограничивающих растворов)
Метод ограничивающих растворов используют в том случае, если концентрация определяемого компонента в анализируемом растворе приблизительно известна и попадает в интервал линейной зависимости показаний прибора (аналитический сигнал) от концентрации. Этим методом пользуются после установления линейности градуировочного графика в определенном диапазоне концентраций.
Результат анализа представляют в форме среднего значения из серии параллельных определений с рассчитанным доверительным интервалом:
Подробные рекомендации и примеры по проведению и оформлению расчетов приведены в пособии [3].
Округление результата определенияx ср ± δ выполняют на последней стадии обработки результатов и начинают с округления значения погрешности δ, а не среднего значения.
Погрешность результата определения δ принято записывать одной цифрой одной или двумя значащими цифрами:
– однойцифрой, если первая цифра погрешности равна 3 или более.
– двумяцифрами, если первая из них равна 1 или 2.
Результат определения x ср должен заканчиваться цифрой того же разряда, что и последняя значащая цифра погрешности. Например, 20,5 ± 0,4; 0,2236 ± 0, 0015; 10,00 ± 0,24.
Обработанные результаты определения представляют в виде таблицы 1.1.
2. ПОТЕНЦИОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Потенциометрические методы анализа основаны на измерении разности потенциалов (ЭДС) между двумя электродами, опущенными в анализируемый раствор. Один электрод является индикаторным, его потенциал зависит от концентрации (активности) определяемого иона. Потенциал другого электрода, который называется электродом сравнения, не зависит от концентрации определяемого иона и в процессе определения остается постоянным. Зависимость равновесного потенциала индикаторного электрода от активности иона в растворе описывается уравнением Нернста:
В потенциометрии используют два вида индикаторных электродов.
1. Электроды, на поверхности которых или в приэлектродном слое протекают электронообменные процессы. К ним относятся инертные электроды (платиновый, золотой) и металлические электроды 1-го рода (серебряный, медный и др.).
2. Электроды, у которых на межфазных границах (мембрана – раствор) протекают ионообменные процессы – ионоселективные (мембранные) электроды (ИСЭ).
В качестве электрода сравнения в лабораторной практике чаще всего используют электрод 2-го рода – хлоридсеребряный.
Потенциометрические методы разделяют на две группы: методы прямой потенциометрии (ионометрия) и методы косвенной потенциометрии (потенциометрическое титрование).
Основным условием выполнения определения потенциометрическим методом является правильный выбор индикаторного электрода. В прямой потенциометрии используют ионоселективные электроды. При потенциометрическом титровании выбор индикаторного электрода зависит от природы определяемого иона и типа химической реакции при титровании.
Метод градуированного графика
Для определения содержания вещества методом градуи-ровочного графика готовят серию из 5-8 стандартных растворов разных концентраций (не менее 3 параллельных растворов для каждой точки).
При выборе интервала концентраций стандартных растворов руководствуются следующими положениями:
• он должен охватывать область возможных изменений концентраций исследуемого раствора, желательно, чтобы оптическая плотность исследуемого раствора соответствовала примерно середине градуировочной кривой;
• желательно, чтобы в этом интервале концентраций при выбранных толщины кюветы I и аналитической длины волны лсоблюдался основной закон светопоглощения, т. е. график D = /(С) был линейным;
• интервал рабочих значений D, соответствующий интервалу стандартных растворов, должен обеспечивать максимальную воспроизводимость результатов измерений.
При совокупности перечисленных условий измеряют оптические плотности стандартных растворов относительно растворителя и строят график зависимости D = /(С).
Полученная кривая называется градуировочной (градуи-ровочным графиком).
Определив оптическую плотность раствора Dx, находят ее значения на оси ординат, а затем на оси абсцисс — соответствующее ей значение концентрации Сх. Этот метод применяют при выполнении серийных фотометрических анализов.
Метод добавок
Метод добавок представляет собой разновидность метода сравнения. Определение концентрации раствора этим методом основано на сравнении оптической плотности исследуемого раствора и того же раствора с добавкой известного количества определяемого вещества. Метод добавок обычно применяют для упрощения работы, для устранения мешающего влияния посторонних примесей, в ряде случаев для оценки правильности методики фотометрического определения. Метод добавок требует обязательного соблюдения основного закона светопоглощения.
Неизвестную концентрацию находят расчетным или графическим способами.
При соблюдении основного закона светопоглощения и постоянной толщине слоя отношение оптических плоскостей исследуемого раствора и исследуемого раствора с добавкой будет равно отношению их концентраций:
где Dx — оптическая плотность исследуемого раствора;
Dx + a — оптическая плотность исследуемого раствора с добавкой;
Сх — неизвестная концентрация исследуемого вещества в исследуемом окрашенном растворе;
Са — концентрация добавки в исследуемом растворе.
Источник:http://www.znaytovar.ru/new117.html
Метод градуировочного графика. Для определения содержания вещества методом градуировочного графика при выбранных оптимальных условиях обычно готовят серию не менее чем из 5 стандартных растворов разных концентраций (не менее 3 параллельных растворов для каждой точки).
При выборе интервала концентраций стандартных растворов руководствуются следующими положениями:
1) интервал должен охватывать область возможных изменений концентраций исследуемого раствора; желательно, чтобы оптическая плотность исследуемого раствора соответствовала примерно середине градуировочной кривой;
2) желательно, чтобы в этом интервале концентраций при выбранных толщине кюветы (l) и аналитической длине волны l * (в большинстве случаев l = l макссветопоглощающего соединения) соблюдался основной закон светопоглощения, т. е. график А = f(c) был прямолинейным;
При совокупности перечисленных условий измеряют оптические плотности стандартных растворов относительно растворителя и строят график зависимости А = f(с). Полученная кривая (рис. 14.4.18) называется градуировочной (градуировочным графиком). Периодически (раз в неделю или реже) ее проверяют по двум-трем свежеприготовленным стандартным растворам.
Рис. 14.4.18. Градуировочный график
Вопрос № 9 условия ф.о
Для достижения высокой воспроизводимости и правильности результатов фотометрического анализа важное значение имеют селективность выбранного реагента и условия проведения фотометрических определений.
Выбор реагента
Для оценки специфических реагентов используют критерии, сформулированные А.К. Бабко [19]. Лучшим реагентом при прочих равных условиях считают такой, который при образовании окрашенного соединения обеспечивает:
1. Наибольшее смещение максимума поглощения D l = l к – l R (где l к и l R — длины волн максимального поглощения комплекса и реагента), характеризующее контрастность реакции. Контрастность фотометрической реакции считается достаточно высокой, если обеспечивается D l = l к – l R ³ 100 нм.
2. Наибольшие абсолютное и относительное изменения молярного коэффициента светопоглощения: D e = e к – e R и 
В тех случаях, когда молярные коэффициенты светопоглощения комплекса и реагента неизвестны, реагенты выбирают по наибольшей разности между суммарной оптической плотностью раствора Асм и оптической плотностью реагента: D А = Асм – АR.
3. Наибольшую разность в значениях рН при образовании окрашенных форм комплекса и реагента: D рН = рНк – рНR.
4. Наибольший интервал значений рН, в котором соблюдается постоянство оптической плотности раствора.
Практическим критерием чувствительности реагента служит угол наклона прямой, характеризующей зависимость оптической плотности (или разности оптических плотностей) от концентрации окрашенного вещества. Графическая, зависимость определяется при длине волны, где значение А (или D А) является максимальным. Чем больше угол наклона (или тангенс угла наклона) этой прямой, тем чувствительнее реагент.
Аналогично по тем же критериям можно оценивать селективные и групповые фотометрические реагенты, но их практическое применение для определения отдельных элементов возможно только в отсутствие мешающих компонентов либо в специальных условиях, при которых мешающее влияние сопутствующих элементов проявляется в незначительной степени.
В тех случаях, когда фотометрическая реакция характеризуется невысокой контрастностью и при выбранной длине волны наблюдается светопоглощение не только анализируемого комплекса, но и фотометрического реагента, находят разность оптических плотностей анализируемого комплекса и чистого реагента при той же концентрации, что и в анализируемом растворе.
Однако эту разность оптической плотности можно отождествлять с оптической плотностью раствора светопоглощающего комплекса только в тех случаях, когда светопоглощение комплекса и реагента обусловлено разными хромофорными группами, что на практике встречается сравнительно редко. Если светопоглощение комплекса и реагента обусловлено одной и той же функциональной группой, то этот прием можно использовать только в условиях большого избытка реагента, когда концентрацией реагента, затраченной на комплексообразование, можно пренебречь.