Гормональная терапия в лечении онкологии
Гормональная терапия является эффективным методом лечения онкологии, однако обладает рядом серьезных побочных эффектов. Онколог медицинского центра «Анадолу», профессор Сердар Турхал рассказал, что это за новый метод и на что пациентам стоит обращать внимание перед началом гормонотерапии.
Что такое гормонотерапия?
Гормоны — это биологически активные вещества, вырабатываемые организмом, которые контролируют рост клеток. Некоторые органы нашего тела нуждаются в половых гормонах, таких как эстроген и тестостерон, для нормального функционирования и развития. Кроме того, существуют гормоны щитовидной железы, а также гормон инсулина, которые выполняют различные функции. Развитие некоторых видов онкологии также может быть обусловлено действием гормонов. Поэтому в их лечении применяются препараты, которые нарушают, блокируют и прекращают их работу. Такой вид лечения называется «гормональной терапией».
При каких видах рака может применяться гормонотерапия?
Гормональная или антигормональная терапия применяется при раке предстательной железы, раке молочной железы, гинекологических онкологических заболеваний. Но она является неэффективной в лечении таких видов онкологии, как рак легких, рак толстой кишки и желудка, потому что они не зависят от гормонов.
Имеются ли побочные эффекты при гормонотерапии?
Гормонотерапия имеет побочные эффекты, и некоторые из них могут быть достаточно серьезными. При раке простаты она может привести к снижению сексуального влечения, возникновению эректильной дисфункции, появлению остеопороза, усталости, набору веса и потере внимания. При раке молочной железы гормональная терапия может вызвать сухость во влагалище, воспаление, привести к снижению сексуального желания, вызвать усталость, тошноту, боль в мышцах и суставах, ломкость костей, остеопороз, реже — свертывание крови, что может стать причиной паралича. Количество побочных эффектов может разным. В связи с этим перед тем, как начинать гормонотерапию, очень важно знать, какие могут возникнуть побочные эффекты, и соотнести их с эффективностью лечения.
Подавляется ли иммунитет при гормонотерапии?
Несмотря на то, что гормонотерапия имеет много побочных эффектов, на иммунную систему она не влияет. Поэтому нет необходимости принимать дополнительные препараты для укрепления иммунитета. Тем не менее перед началом лечения следует тщательно изучить побочные эффекты, а также проконсультироваться со своим лечащим врачом о том, как с ними бороться. Если они усиливаются или продолжаются длительное время, несмотря на все предпринимаемые меры, необходимо снова обратиться к врачу. Лечение побочных эффектов не ограничивается приемом лекарственных средств. Например, при ослаблении костной ткани (остеопорозе) определенные упражнения могут тоже быть полезны. Также может быть рекомендован прием кальция и витаминно-минеральных добавок.
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
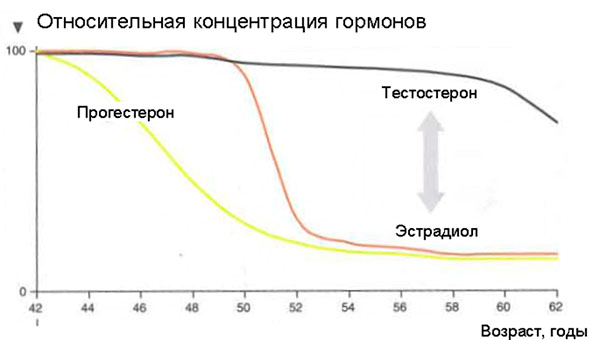
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
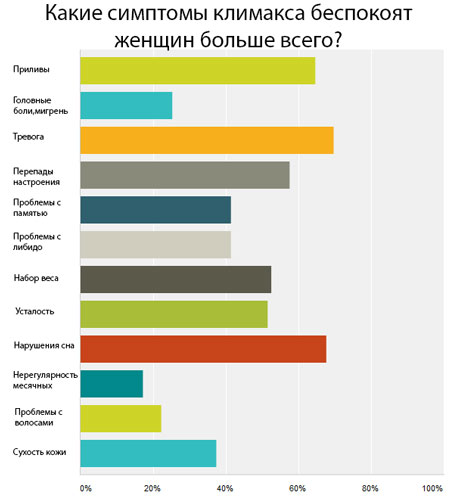
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
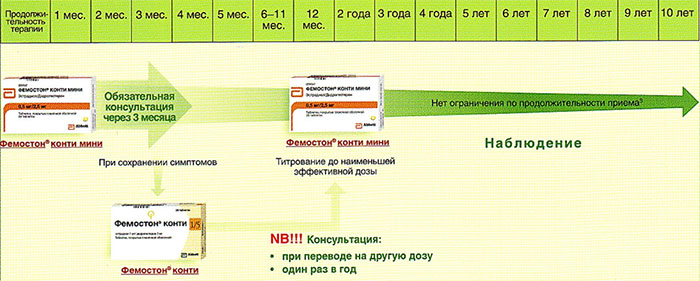
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
Препараты для монофазной терапии – когда месячные отсутствуют
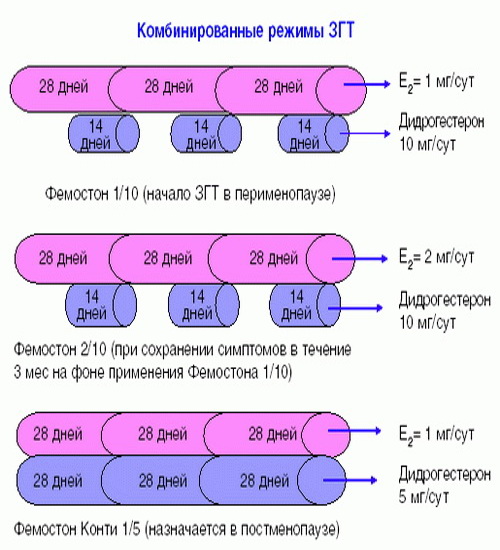
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
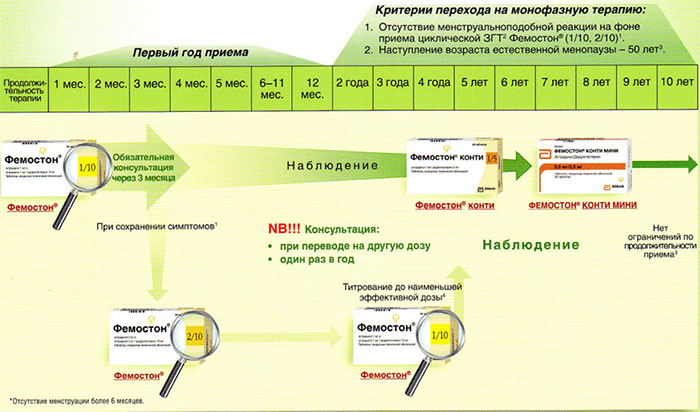
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Заместительная гормонотерапия и злокачественные опухоли
Одним из сдерживающих моментов при назначении ЗГТ является риск возникновения злокачественных опухолей, особенно рака молочной железы и половых органов. Злокачественные опухоли репродуктивных органов составляют от 35 до 45% в структуре онкологической забо
А. Ф. Урманчеева, доктор медицинских наук
М. М. Бурнина
Медицинская академия последипломного образования, Санкт-Петербург
Одним из сдерживающих моментов при назначении ЗГТ является риск возникновения злокачественных опухолей, особенно рака молочной железы и половых органов. Злокачественные опухоли репродуктивных органов составляют от 35 до 45% в структуре онкологической заболеваемости женщин в развитых странах. В России в 1997 году у 210 144 женщин впервые в жизни было диагностировано злокачественное новообразование, подавляющее большинство заболевших было в возрасте 60-69 лет. Рак молочной железы лидирует в структуре онкологической заболеваемости, его удельный вес составил 18,4%, гинекологический рак занимает второе место (17,0%), третье место принадлежит колоректальному раку (11,2%) и четвертое — раку желудка (9,9%).
За последние годы в мире накоплен значительный опыт применения ЗГТ, что позволяет провести анализ некоторых исследований и сделать соответствующие выводы о возможном риске заболевания злокачественными опухолями в женской популяции, а также о применении ЗГТ у онкологических пациенток.
Рак молочной железы (РМЖ). В течение многих лет причину развития РМЖ связывали исключительно с избыточной продукцией эстрогенов или некоторых их фракций. В пользу «эстрогенной» гипотезы свидетельствуют полученные в эксперименте на животных опухоли молочной железы под воздействием химических канцерогенов при одновременном введении эстрогенов, а также случаи регресса первичной опухоли и метастазов РМЖ после овариоэктомии. Многочисленные эпидемиологические исследования также косвенно указывают на роль яичников в развитии РМЖ. Так, РМЖ чаще развивается у не беременевших, не рожавших, мало рожавших или поздно рожавших женщин (после 30 лет). Риск РМЖ увеличивается у женщин с ранним менархе (до 12 лет) и поздней менопаузой (после 50 лет). В последние годы длительность репродуктивного периода увеличилась в два раза (с 15-20 лет до 20-40 лет) при сокращении числа родов, образовалось так называемое «эстрогенное окно». Тем не менее, несмотря на многочисленные свидетельства о причастности эстрогенов к развитию РМЖ, по мнению ведущих специалистов, эстрогены не являются канцерогенами в классическом смысле этого слова. Нет ни одного убедительного научного исследования, показавшего наличие высокого уровня классических эстрогенов у больных РМЖ по сравнению со здоровыми женщинами соответствующего возраста. Очевидно, для возникновения и роста РМЖ не обязательна избыточная продукция эстрогенов, достаточно их присутствие в обычных физиологических уровнях соответственно возрасту. Канцерогенез представляет собой многостадийный процесс, и отдельный единовременный фактор не способен вызвать рак. В связи с этим в последние годы эстрогенам отводится соответствующая роль на стадии развития уже инициированного опухолевого процесса. Кроме того, необходимо помнить также об открытии в 90-х годах генов BRCA1 и BRCA2, что внесло ясность в наследственные формы у 10% больных РМЖ.
Результаты опубликованных с 1970 года более 50 когортных эпидемиологических исследований (выборочных, нерандомизированных) о ЗГТ и РМЖ были крайне противоречивыми и несопоставимыми по численности обследуемых и составу препаратов. Проведенные в 90-е годы метанализы этих исследований показали, что прием ЗГТ в период времени до 5 лет не увеличивал риск РМЖ, тогда как более длительное назначение способствовало росту РМЖ. Последний наиболее полный реанализ 51-го эпидемиологического исследования, охватывающего 52 тыс. больных РМЖ и 108 тыс. женщин без РМЖ, показал, что относительный риск РМЖ составляет 1,31% для женщин, принимавших ЗГТ в течение 5 лет и более. Риск одинаков для различных видов применяемых эстрогенов (конъюгированных или 17b-эстрадиола). С 1980 года с целью протективного действия на эндометрий в ЗГТ применяются прогестагены как в циклическом, так и в постоянном режиме. В первом крупномасштабном исследовании, проведенном в США, по комбинированной ЗГТ не было установлено увеличение риска РМЖ при добавлении прогестинов, хотя дальнейший метанализ выявил относительный риск при длительной (более 5 лет) комбинированной ЗГТ в странах Европы и США. В то же время в клиниках, где проводился опрос больных РМЖ, число пациенток, получавших ранее ЗГТ, было таким же, как и в общей женской популяции страны. Анализируя случаи РМЖ, развившиеся у пациенток, длительно принимавших ЗГТ, все клиницисты отмечают более прогностически благоприятное течение заболевания за счет высокой дифференцировки опухоли, меньших размеров и низкой потенции к метастазированию по сравнению с РМЖ у больных, ранее не получавших ЗГТ. Таким образом, ЗГТ длительностью до 5 лет не увеличивает риск РМЖ, но, учитывая повышение вероятности РМЖ при долговременной ЗГТ (более 5 лет), необходимо рекомендовать маммографию до начала ЗГТ и далее ежегодно. При этом надо помнить, что интерпретация маммограмм может быть затруднена из-за увеличения плотности ткани молочной железы на фоне ЗГТ.
Дискуссионным является вопрос о назначении ЗГТ больным РМЖ после излечения. Однако в настоящее время уже накоплен некоторый опыт в лечении климактерических расстройств у пациенток, ранее подвергавшихся лечению по поводу РМЖ. Несколько ретроспективных анализов исследований, включавших от 25, 65, 77 до 146 больных РМЖ, не выявили ухудшения прогноза заболевания, т. е. увеличения риска рецидивов заболевания по сравнению с контрольными группами больных РМЖ, не получавших ЗГТ. Исходя из этого, авторы полагают, что недлительная ЗГТ может быть назначена больным РМЖ, имевшим начальные формы рака без метастатического поражения лимфатических узлов. Однако учитывая тот факт, что длительная ЗГТ (более 5 лет) увеличивает риск РМЖ в популяции в 1,3-1,4 раза, необходимы рандомизированные исследования по ЗГТ больным РМЖ. Такого рода пилотное исследование запланировано в Англии и Италии. Нужно также отметить, что у больных, излечившихся от РМЖ, в два-пять раза выше риск развития РМЖ контрлатеральной молочной железы, а у женщин, у которых РМЖ был в молодом возрасте, — в десять раз.
Гинекологический рак
Рак эндометрия (РЭ). В 70-е годы была отмечена отчетливая взаимосвязь между эстрогенной ЗГТ (ЭЗГТ) и увеличением риска РЭ. Впоследствии метанализ различных исследований позволил уточнить эту взаимосвязь; относительный риск сохранялся у больных, получавших эстрогены, и был минимален для не получавших. Риск РЭ возрастал в зависимости от длительности приема эстрогенов: от 1,4 при приеме менее 1 года до 9,5% при длительности более 10 лет. После прекращения приема эстрогенов риск снижался к концу второго года до показателей, отмеченных у больных, не использовавших ЭЗГТ, хотя он мог оставаться более высоким в течение 10 лет после прекращения ЭЗГТ. В дальнейшем с целью защиты эндометрия от пролиферативного влияния эстрогенов в ЗГТ были включены прогестины. При добавлении прогестинов риск РЭ зависел от длительности приема прогестинов: менее 10 дней он был 2,4%, более 10 дней — 1,1%, т. е. сохранялся на том же уровне, что и у использующих комбинированную ЗГТ. Хотя, по данным Бересдорфа, длительная комбинированная ЗГТ (5 лет и более) увеличивает риск РЭ в два раза, РЭ, развившийся на фоне ЗГТ, так же как и РМЖ, протекает менее агрессивно (в большинстве случаев он высокодифференцированный, стадии IA), и риск смерти от РЭ значительно ниже у пациентов, получавших ЗГТ, чем у не получавших.
Другим спорным моментом остается вопрос о применении ЗГТ больными РЭ после радикального лечения. К 1998 году были известны три когортных исследования по применению ЗГТ больным РЭ (153 человека) после радикальных экстирпаций матки с придатками. Анализ, проведенный в 1999 году, касается еще 130 больных РЭ, получавших ЭЗГТ. Как и предыдущие научные изыскания, он не выявил увеличения риска рецидивов РЭ, однако для окончательного утверждения также необходимы рандомизированные исследования. Следует считать, что ЗГТ может быть назначена больным РЭ с благоприятным прогнозом при безрецидивном периоде более 5 лет после радикального лечения, а также больным саркомой матки, исключая эндометрильностромальные формы.
Рак яичника (РЯ). Более чем в 300 публикациях по ЗГТ и РЯ не отмечено роста заболеваемости РЯ на фоне приема ЗГТ. Только в девяти работах говорится о некотором увеличении риска при длительной ЗГТ. В то же время клиническое исследование, проведенное Гвидоззи, Папонтом среди 130 больных РЯ, части из которых в послеоперационном периоде назначалась ЭЗГТ в течение 6-8 недель, не выявило ее негативного влияния на безрецидивный интервал и общую выживаемость по сравнению с лечением без ЭЗГТ.
Рак шейки матки (РШМ). РШМ не является гормонозависимой опухолью, в его этиологии основная роль отводится папилломавирусной инфекции, передающейся половым путем. При ретроспективном анализе риск инвазивного рака шейки матки у женщин, принимавших ЗГТ, оказался ниже, чем в общей популяции. Возможно, это связано с более тщательным скринингом, проводимым среди пациенток, которым назначается ЗГТ. Больным, подвергавшимся хирургическому вмешательству в объеме радикальных расширенных экстирпаций матки с придатками по поводу РШМ, как правило, назначается ЭЗГТ для ликвидации явлений постовариэктомического синдрома. Наш небольшой опыт ЗГТ диветреном (эстрадиол валерат + медроксипрогестерон ацетат) и дивигелем (17b-эстрадиол) среди больных РШМ (21 человек) в различные сроки после хирургического или комбинированного лечения (операция + облучение) представлен в табл. 1, 2. После шестимесячного приема препаратов модифицированный менопаузальный индекс (ММИ) снизился более чем на 40% (на 45,0% — при приеме дивитрена и на 42,4% — дивигеля). Положительная динамика в лечении постовариэктомического синдрома характеризовалась в первую очередь снижением почти на 50% выраженности психоэмоциональных и нейровегетативных симптомов. Изменение ММИ при оценке метаболических изменений также указывало на положительный эффект ЗГТ. Тем не менее сохранялись урогенитальные расстройства, свойственные не столько урогенитальному синдрому, сколько особенностям лечения рака шейки матки (радикализм операции в сочетании с лучевой терапией). Степень их выраженности, однако, значительно снижалась за счет исчезновения дизурических явлений, диспареунии, недержания мочи, никтурии. При исследовании гормонального спектра у 11 больных, получавших дивитрен, отмечено снижение на 20% уровня ФСГ при одновременном повышении на 90% уровня эстрадиола. При оценке липидного спектра крови установлено, что его показатели через 6 месяцев после начала лечения статистически не отличались от исходных. Благоприятным фактором, указывающим на безопасность данного метода лечения, является и снижение атерогенного индекса на 20%. Ни у кого из пациенток за время проведения ЗГТ и далее в течение последующих 12 месяцев не отмечено рецидива заболевания. По данным Плоха, пятилетняя выживаемость больных РШМ, получавших ЗГТ и не получавших ЗГТ, была одинаковой. В настоящее время в наших онкологических клиниках больным РШМ (более 60 человек) после радикального хирургического лечения уже в раннем послеоперационном периоде назначается ЗГТ дивигелем, эстрофемом, прогиновой, климара или комбинированная ЗГТ фемостоном, цикло-прогиновой, клименом, дивиной.
Рак вульвы и влагалища. Плоскоклеточный рак вульвы и влагалища, так же как и РШМ, не является гормонозависимым и развивается у женщин пожилого и старческого возраста. Работ по применению ЗГТ у больных раком вульвы и влагалища не проводилось.
Негинекологический рак
Во всех исследованиях по изучению риска колоректального рака на фоне ЗГТ отмечается статистически достоверное снижение на 30-40% заболеваемости среди получавших ЗГТ. В опубликованном в 1996 году в Швеции отчете о статистическом исследовании заболеваемости и смертности среди женщин, получавших и не получавших ЗГТ, также указывается на значительное снижение заболеваемости колоректальным раком, небольшое снижение частоты гепатоцеллюлярного и церебрального рака и отсутствие влияния ЗГТ на частоту меланом, рака легкого и почек.
Представленные материалы свидетельствуют о возможности широкого применения ЗГТ не только в общей женской популяции, но и в реабилитации части онкологических больных после их излечения при тщательном динамическом наблюдении. Тем не менее необходимо продолжение кооперированных научно-клинических исследований по изучению онкологических аспектов ЗГТ.